Структура, својства, номенклатура и употреба златног оксида (ИИИ) (Ау2О3)
Тхе златни оксид (ИИИ) је неорганско једињење чија је хемијска формула Ау2О3. Теоретски, може се очекивати да је његова природа ковалентног типа. Међутим, присуство одређеног јонског карактера у његовој чврстини не може се потпуно одбацити; или оно што је исто, претпоставимо одсуство лиценце3+ поред аниона О2-.
Можда изгледа контрадикторно да злато, као племенити метал, може да зарђа. У нормалним условима, делови злата (као и звезде на слици испод) не могу бити оксидовани контактом са кисеоником у атмосфери; међутим, када је озрачена ултраљубичастим зрачењем у присуству озона, ОР3, слика је другачија.

Да су златне звезде биле подвргнуте овим условима, оне би се претвориле у црвенкастосмеђу, карактеристичну за Ау2О3.
Друге методе за добијање овог оксида би укључивале хемијску обраду наведених звезда; на пример, претварање златне масе у одговарајући хлорид, АуЦл3.
После, до АуЦл3, и остатак могућих соли насталих од злата, додан је јак базични медијум; и са овим добијате хидрирани оксид или хидроксид, Ау (ОХ)3. Коначно, ово последње једињење се термички дехидрира да би се добила Ау2О3.
Индек
- 1 Структура златног оксида (ИИИ)
- 1.1 Електронски аспекти
- 1.2 Хидрати
- 2 Својства
- 2.1 Физички изглед
- 2.2 Молекулска маса
- 2.3 Густина
- 2.4 Тачка топљења
- 2.5 Стабилност
- 2.6 Растворљивост
- 3 Номенклатура
- 4 Усес
- 4.1 Бојење наочара
- 4.2 Синтеза аурата и фулминирајућег злата
- 4.3 Руковање самосталним слојевима
- 5 Референце
Структура златног оксида (ИИИ)
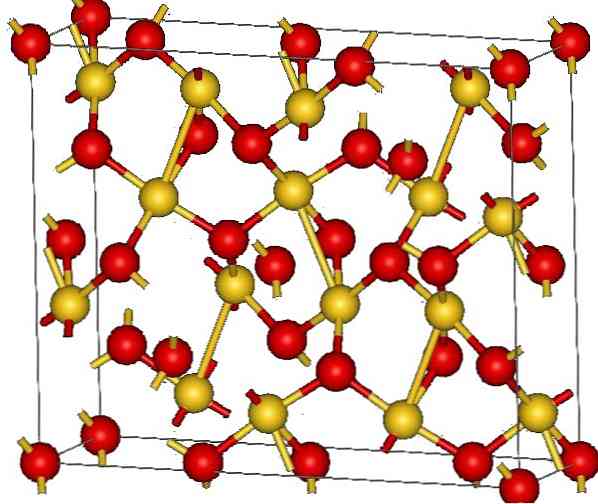
Кристална структура злата (ИИИ) оксида је приказана на горњој слици. Приказан је распоред атома злата и кисеоника у чврстом материјалу, било као неутрални атоми (ковалентна чврста материја), или као јони (јонска чврста материја). Нејасно је довољно елиминирати или поставити Ау-О везе у сваком случају.
Према слици, претпоставља се да ковалентни карактер доминира (што би било логично). Из тог разлога, представљени атоми и везе су приказани са сферама и баровима. Златне сфере одговарају атомима злата (АуИИИ-О), и црвенкасте до атома кисеоника.
Ако пажљиво погледате, видећете да постоје АуО јединице4, који су спојени атомима кисеоника. Други начин да се визуализује би био да се размотри свака Ау3+ је окружен са четири О2-; Наравно, из јонске перспективе.
Ова структура је кристална, јер су атоми поређани у истом далекометном узорку. Тако, његова унитарна ћелија одговара ромбоедарном кристалном систему (исто као и на горњој слици). Дакле, све Ау2О3 може се изградити да су све те сфере ћелијске јединице расподељене у простору.
Електронски аспекти
Злато је прелазни метал и за очекивати је да његове 5д орбитале директно утичу на 2п орбитале атома кисеоника. Ово преклапање њихових орбитала би теоретски требало да генерише проводне траке, које би претвориле Ау2О3 у чврстом полупроводнику.
Дакле, права структура Ау2О3 то је још сложеније с тим на уму.
Хидрати
Златни оксид може задржати молекуле воде унутар својих ромбоедричних кристала, што доводи до хидрата. Када се такви хидрати формирају, структура постаје аморфна, тј. Неуређена.
Хемијска формула за такве хидрате може бити било која од следећих, која у ствари није дубоко разјашњена: Ау2О3Х зХ2О (з = 1, 2, 3, итд.), Ау (ОХ)3, или АукОи(ОХ)з.
Формула Ау (ОХ)3 представља прекомерно поједностављивање праве композиције наведених хидрата. То је зато што су унутар златног хидроксида (ИИИ) истраживачи такође пронашли присуство Ау2О3; и стога, има смисла третирати га изоловано као "једноставан" хидроксид прелазног метала.
С друге стране, чврсте са формулом АукОи(ОХ)з може се очекивати аморфна структура; јер, то зависи од коефицијената к, и и з, чије би варијације довеле до стварања свих врста структура које једва да показују кристални образац.
Пропертиес
Физички изглед
То је црвенкасто смеђа чврста маса.
Молецулар масс
441,93 г / мол.
Густина
11.34 г / мЛ.
Тачка топљења
Топи се и разграђује на 160ºЦ. Због тога нема тачке кључања, тако да овај оксид никада не досеже тачку кључања.
Стабилност
Тхе Ау2О3 она је термодинамички нестабилна, јер, као што је речено на почетку, злато нема тенденцију оксидације у нормалним температурним условима. Тако се лако редукује да постане поново племенито злато.
Што је температура виша, то је бржа реакција, позната као термичка разградња. Дакле, Ау2О3 на 160 ° Ц разграђује се да производи метално злато и ослобађа молекуларни кисеоник:
2 Ау2О3 => 4 Ау + 3 О2
Веома слична реакција се може појавити са другим једињењима која погодују поменутој редукцији. Зашто смањење? Зато што се злато враћа да добије електроне које му је кисеоник одузео; што је исто као да каже да губи везу са кисеоником.
Растворљивост
То је чврста материја нерастворљива у води. Међутим, раствара се у хлороводоничној киселини и азотној киселини, због формирања хлорида и нитрата злата.
Номенклатура
Златни оксид (ИИИ) је назив који се уређује номенклатуром залиха. Други начини да то поменете су:
-Традиционална номенклатура: аурерични оксид, јер је валенција 3+ највиша за злато.
-Систематска номенклатура: диоро триоксид.
Усес
Бојање наочара
Једна од његових најистакнутијих примена је да обезбеди црвенкасте боје одређеним материјалима, као што су наочаре, поред додељивања одређених својстава својствених атомима злата..
Синтеза аурата и експлозивног злата
Ако се дода Ау2О3 у медијум где је растворљив, а у присуству метала, аурати могу да се таложе након додавања јаке базе; који су формирани од АуО аниона4- у друштву металних катиона.
Такође, Ау2О3 реагује са амонијаком да би се формирало златно пуњење, Ау2О3(НХ3)4. Његово име потиче од чињенице да је веома експлозивно.
Руковање самосталним слојевима
На злато и његов оксид, одређена једињења, као што су диалкил дисулфиди, РССР, се не адсорбују на исти начин. Када дође до ове адсорпције, спонтано се формира Ау-С веза, где атом сумпора показује и дефинише хемијске карактеристике наведене површине у зависности од функционалне групе на коју је везан..
РССР се не може адсорбовати на Ау2О3, али на металном злату. Дакле, ако се модификује површина злата и његов степен оксидације, као и величина честица или слојева Ау2О3, може бити дизајнирана више хетерогена површина.
Ова површина Ау2О3-АуСР је у интеракцији са металним оксидима одређених електронских уређаја, развијајући тако будуће паметније површине.
Референце
- Википедиа. (2018). Голд (ИИИ) оксид. Преузето са: ен.википедиа.орг
- Цхемицал Формулатион (2018). Златни оксид (ИИИ). Опорављен од: формулационкуимица.цом
- Д. Мицхауд. (24. октобар 2016. године). Голд окидес. 911 Металлургист. Добављено из: 911металлургист.цом
- Схи, Р. Асахи и Ц. Стампфл. (2007). Својства златних оксида Ау2О3 анд Ау2О: Истрага о првим принципима. Америчко физичко друштво.
- Цоок, Кевин М. (2013). Златни оксид као слој маскирања за региоселективну површинску хемију. Тезе и дисертације. Папер 1460.


