Структура, својства, номенклатура, употреба сребро сулфидне (Аг2С) структуре
Тхе сребрни сулфид је неорганско једињење чија је хемијска формула Аг2С. Састоји се од црно-сивкасте чврсте масе формиране Аг катионима+ и аниони С2- у односу 2: 1. Тхе С2- веома је слично Аг+, јер су оба мека иона и успевају да се стабилизују једни са другима.
Сребрни украси имају тенденцију да потамне, изгубивши свој карактеристичан сјај. Промена боје није производ оксидације сребра, већ његова реакција са сумпороводом који је присутан у околини при ниским концентрацијама; Ово може доћи од труљења или деградације биљака, животиња или хране богате сумпором.

Тхе Х2С, чији молекул носи атом сумпора, реагује са сребром према следећој хемијској једначини: 2Аг (с) + Х2С (г) => Аг2С (с) + Х2(г)
Дакле, Аг2С је одговоран за црне слојеве формиране на сребру. Међутим, у природи се овај сумпор може наћи иу минералима акантита и аргентите. Два минерала се разликују од многих других по својим црним и светлим кристалима, као што је то случај са чврстим делом на горњој слици.
Тхе Аг2С представља полиморфне структуре, атрактивне електронске и оптоелектронске особине, је полупроводник и обећава да ће бити материјал за развој фотонапонских уређаја, као што су соларне ћелије.
Индек
- 1 Струцтуре
- 2 Својства
- 2.1 Молекуларна тежина
- 2.2 Изглед
- 2.3 Мирис
- 2.4 Тачка топљења
- 2.5 Растворљивост
- 2.6 Структура
- 2.7 Индекс рефракције
- 2.8 Диелектрична константа
- 2.9 Електроника
- 2.10 Реакција редукције
- 3 Номенклатура
- 3.1 Систематика
- 3.2 Стоцк
- 3.3 Традиционални
- 4 Усес
- 5 Референце
Структура
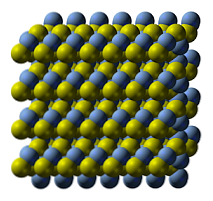
Кристална структура сребрног сулфида је приказана на горњој слици. Плаве сфере одговарају Аг катионима+, док су жуте до аниона С2-. Тхе Аг2С је полиморфан, што значи да може усвојити неколико кристалних система под одређеним температурним условима.
Како? Кроз фазну транзицију. Иони су преуређени на такав начин да повећање температуре и вибрације чврстог материјала не нарушавају равнотежу електростатичке привлачности и одбијања. Када се то догоди, каже се да постоји фазни прелаз, и стога чврсти материјал показује нове физичке особине (као што су сјај и боја)..
Тхе Аг2С при нормалним температурама (нижим од 179ºЦ), има моноклинску кристалну структуру (α- Аг2С). Поред ове чврсте фазе постоје још два: бцц (кубични центар у телу) између 179 до 586ºЦ, и фцц (кубични центриран у лицима) на веома високим температурама (δ- Аг).2С).
Аргентитски минерал се састоји од фцц фазе, познате и као β-Аг2С. Када се охлади и претвори у литицу, њихове структурне карактеристике преовлађују у комбинацији. Дакле, обје кристалне структуре коегзистирају: моноклинску и бцц. Дакле, појављују се црне чврсте материје са светлим и занимљивим призвуком.
Пропертиес
Молекуларна тежина
247,80 г / мол
Изглед
Сиви црни кристали
Мирис
Тоалет.
Тачка топљења
836ºЦ. Ова вредност се слаже са чињеницом да је Аг2С је једињење са мало јонског карактера и стога се топи на температурама испод 1000ºЦ.
Растворљивост
У води само 6,21. 10-15 г / Л на 25ºЦ. То јест, количина црне чврсте супстанце која је солубилизована је занемарива. Ово је, опет, последица малог поларног карактера Аг-С везе, где нема значајне разлике електронегативности између оба атома..
Такође, Аг2С је нерастворљив у свим растварачима. Ниједан молекул не може ефикасно да раздвоји своје кристалне слојеве у Аг ионима+ и С2- солватед.
Структура
Четири слоја С-Аг-С веза такође се могу видети на слици структуре, која се крећу један преко другог када је чврста материја подложна разумевању. Ово понашање значи да је, упркос томе што је полупроводник, дуктилан као и многи метали на собној температури.
С-Аг-С слојеви се правилно уклапају због њихове угаоне геометрије које се посматрају као цик-цак. Имајући снагу разумевања, они се крећу на оси померања и тако изазивају нове нековалентне интеракције између атома сребра и сумпора.
Рефрацтиве индек
2.2
Диелектрична константа
6
Елецтроницс
Тхе Аг2С је амфотерни полупроводник, тј. Понаша се као да је типа н и типа п. Такође није крхак, па је проучаван за његову примену у електронским уређајима.
Реакција редукције
Тхе Аг2С може се редуковати на металик сребро купањем црних комада топлом водом, НаОХ, алуминијумом и соли. Следећа реакција се одвија:
3Аг2С (с) + 2Ал (с) + 3Х2О (л) => 6Аг (с) + 3Х2С (ац) + Ал2О3(с)
Номенклатура
Силвер, чија је електронска конфигурација [Кр] 4д105с1, може да изгуби само један електрон: онај крајње орбиталне 5с. Дакле, Агатион+ остаје са електронском конфигурацијом [Кр] 4д10. Према томе, она има јединствену валенцију од +1, која одређује како треба да се називају њена једињења.
Сулфур, с друге стране, има електронску конфигурацију [Не] 3с23п4, и потребан је два електрона да заврши свој валентни октет. Када добије ова два електрона (од сребра), трансформише се у сумпорни анион, С2-, са конфигурацијом [Ар]. Односно, то је изоелектронски за аргон племенити гас.
Тако да је Аг2С мора бити позван према сљедећим номенклатурама:
Систематика
Мајмунсумпор дисилвер Овде ћемо узети у обзир број атома сваког елемента и означени су префиксима грчких нумератора.
Стоцк
Силвер сулфиде. Када има јединствену валенцију од +1, она није назначена римским бројевима у заградама: сребров сулфид (И); што је нетачно.
Традиционално
Сулфуро аргентицо. Пошто сребро "ради" са валенцом од +1, суфикс -ицо се додаје његовом имену аргентум ин Латин.
Усес
Неке од нових употреба за Аг2С су следеће:
-Боје њихових наночестица (различитих величина) имају антибактеријску активност, нису токсичне и могу се користити у области медицине и биологије..
-Њихове наночестице могу да формирају оно што је познато као квантне тачке. Оне апсорбују и емитују зрачење са већим интензитетом од многих органских флуоресцентних молекула, тако да могу потиснути ово друго као биолошке маркере.
-Структуре α-Аг2С чине га упечатљивим електронским својствима које се могу користити као соларне ћелије. Такође представља полазну тачку за синтезу нових термоелектричних материјала и сензора.
Референце
- Марк Пеплов. (17. април 2018). Полупроводнички сребрни сулфид се протеже као метал. Преузето са: цен.ацс.орг
- Сарадња: Аутори и уредници запремине ИИИ / 17Е-17Ф-41Ц () Силвер сулфидне (Аг2С) кристалне структуре. У: Маделунг О., Росслер У., Сцхулз М. (едс) Не-тетрахедрално везани елементи и бинарни спојеви. Спрингер, Берлин, Хеиделберг.
- Википедиа. (2018). Силвер сулфиде. Такен фром: ен.википедиа.орг
- Станислав И. Садовников & цол. (Јул 2016. године). Аг2С наночестице сребрног сулфида и колоидна раствора: Синтеза и својства. Преузето са: сциенцедирецт.цом
- Азо Материалс. (2018). Силвер Сулфиде (Аг2С) Полупроводници. Преузето из: азом.цом
- А. Нвофе. (2015). Перспективе и изазови танких филмова о сулфиду сребра: преглед. Одсек за науку о материјалима и обновљиву енергију, Одсек за индустријску физику, Ебонии Стате Университи, Абакалики, Нигерија.
- УМассАмхерст. (2011). Демонстрације предавања: чишћење тарнисхед сребра. Преузето из: лецтуредемос.цхем.умасс.еду
- Студија. (2018). Шта је Силвер Сулфиде? - Хемијска формула и употреба. Преузето из: студи.цом


