Процес егзотермне реакције, типови и примери
Тхе егзотермна реакција је врста хемијске реакције у којој долази до преноса енергије, углавном у облику ослобађања топлоте или светлости. Име долази од грчког префикса еко, што значи "у иностранству"; и израз "термални", који се односи на топлоту или температуру.
У том смислу, егзотермне реакције могу пренијети друге врсте енергије у околину у којој се стварају, као што су експлозије и њихов начин пријеноса кинетичке и звучне енергије када се твари које су у плиновитој фази при високим температурама проширују. насилан начин.
На исти начин, у случају коришћења батерија, врши се и егзотермна реакција, само у овом случају се преноси електрична енергија.
Индек
- 1 Процесс
- 2 Типови
- 2.1 Реакције сагоријевања
- 2.2 Реакције неутрализације
- 2.3 Реакције оксидације
- 2.4 Реакција термита
- 2.5 Реакциона полимеризација
- 2.6 Реакција нуклеарне фисије
- 2.7 Остале реакције
- 3 Примери
- 4 Референце
Процес
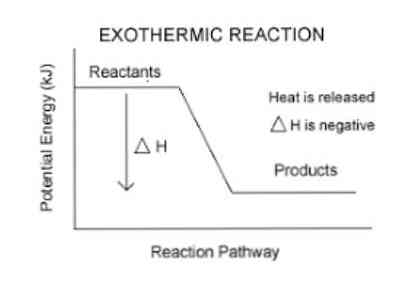
Раније је поменуто да када дође до егзотермне реакције долази до ослобађања енергије, што се може лакше визуализовати у следећој једначини:
Реагенс (и) → Производ (и) + Енергија
Дакле, да би се квантификовала енергија која је апсорбована или ослобођена од стране система, користи се термодинамички параметар који се назива енталпија (означена са "Х"). Ако у систему (у овом случају, хемијској реакцији) долази до ослобађања енергије у околину, онда ће варијација енталпије (изражена као ΔХ) имати негативну вредност.
Иначе, ако је варијација ове мјере позитивна, она одражава апсорпцију топлоте из околине. Такође, величина варијације енталпије система је израз количине енергије која се преноси у или из окружења.
Што је већа величина ΔХ, то је веће ослобађање енергије из система у околни медиј.
То је због тога што је у овим реакцијама нето енергија која се ослобађа када се стварају нове везе већа од нето енергије која се користи у фрагментацији веза.
Из горе наведеног може се закључити да је ова врста реакција веома честа, јер производи реакције имају количину енергије која је ускладиштена у везама која је већа од оне која се налази у реактантима..
Типови
Постоје различите врсте егзотермних реакција у различитим областима хемије, било у лабораторији или у индустрији; неке се спонтано изводе, а другима су потребни специфични услови или нека врста супстанце, као што је катализатор.
Следе најважније врсте егзотермних реакција:
Реакције сагоревања
Реакције сагоревања су оне које имају редок тип, а које се јављају када једна или више супстанци реагују са кисеоником, што генерално доводи до ослобађања светлости и топлотне енергије - то је, светлост и топлота - када се производи пламен..
Неутрализационе реакције
Неутрализационе реакције су карактерисане интеракцијом између киселинских врста и алкалне супстанце (базе) како би се формирала сол и вода, што испољава егзотермичку природу..
Оксидационе реакције
Постоје многе реакције овог типа које показују егзотермно понашање, јер оксидација кисеоника изазива ослобађање велике количине енергије, као што се дешава у оксидацији угљоводоника..
Термите реакција
Ова реакција може произвести температуру од око 3000 ° Ц, а због високог афинитета алуминијумског праха са великим бројем оксида метала, користи се за заваривање челика и гвожђа..
Реакција полимеризације
Овај тип реакције је онај који настаје када одређени број хемијских врста које се називају мономери реагују, што су јединице које се у комбинацији понављају у ланцима да би се формирале макромолекуларне структуре које се називају полимери.
Реакција нуклеарне фисије
Овај процес се односи на поделу језгра атома који се сматра тешким - то јест, са масеним бројем (А) већим од 200 - да би се произвели фрагменти или језгра мање величине са средњом масом..
У овој реакцији, где се формира један или више неутрона, ослобађа се велика количина енергије јер језгро са већом тежином има мању стабилност од својих производа.
Друге реакције
Постоје и друге егзотермне реакције од великог значаја, као што је дехидрација неких угљених хидрата при реакцији са сумпорном киселином, апсорпција воде која има натријум хидроксид изложен отвореном ваздуху или оксидација металних врста у многим реакцијама корозије..
Примери
У наставку су наведени неки примјери егзотермних реакција, које производе варијацију енталпије која има негативну вриједност због чињенице да ослобађају енергију, као што је горе наведено..
На пример, сагоревање пропана је спонтана егзотермна реакција:
Ц3Х8(г) + 5О2(г) → 3ЦО2(г) + 4Х2О (л)
Други случај егзотермног понашања показује реакција неутрализације између натријум карбоната и хлороводоничне киселине:
НаХЦО3(ац) + ХЦл (ац) → НаЦл (ац) + Х2О (л) + ЦО2(г)
Такође је приказана оксидација етанола у сирћетну киселину која се користи у дисајлаторима, чија је комплетна реакција приказана у следећој једначини:
3ЦХ3ЦХ2ОХ + 2К2Цр2О7 + 8Х2СО4 → ЦХ3ЦООХ + 2Цр (СО4)3 + 2К2СО4 + 11Х2О
Друга класа егзотермне реакције је тзв. Термитна реакција, у којој се алуминијум комбинује са металним оксидом, као што је приказано у наставку:
2Ал (с) + Вера2О3(с) → Ал2О3(с) + Фе (л)
Поред горе објашњених примера, постоји широк спектар реакција које се такође сматрају егзотермним, као што је разлагање одређених органских отпадних супстанци за компостирање..
Он такође наглашава оксидацију луциферинског пигмента дејством ензима луциферазе да би произвео биолуминисценцију карактеристичну за кријеснице, па чак и дисање, међу многим другим реакцијама.
Референце
- Википедиа. (с.ф.). Егзотермна реакција. Преузето са ес.википедиа.орг
- ББЦ (с.ф.). Промене енергије и реверзибилне реакције. Преузето са ббц.цо.ук
- Цханг, Р. (2007). Хемија, Девето издање. (МцГрав-Хилл).
- Валкер, Д. (2007). Цхемицал Реацтионс. Преузето са боокс.гоогле.цо.ве
- Саундерс, Н. (2007). Екплоринг Цхемицал Реацтионс. Преузето са боокс.гоогле.цо.ве


