Структура, својства и употреба калцијевог оксида (ЦаО)
Тхе калцијум оксид (ЦаО) је неорганско једињење које садржи калцијум и кисеоник у јонским облицима (не треба мешати са калцијум пероксидом, ЦаО)2). У свету је познат као креч, реч која означава било које неорганско једињење које садржи карбонате, калцијумове оксиде и хидроксиде, као и друге метале као што су силициј, алуминијум и гвожђе..
Овај оксид (или креч) се такође колоквијално помиње као вапно или гашено вапно, зависно од тога да ли је или није хидрирано. Лиме је калцијум оксид, док је гашено вапно његов хидроксид. С друге стране, кречњак (креч или каљено вапно) је заправо седиментна стијена која се састоји углавном од калцијевог карбоната (ЦаЦО)3).

То је један од највећих природних извора калцијума и представља сировину за производњу калцијум оксида. Како се производи овај оксид? Карбонати су подложни термичкој разградњи; загревање калцијум карбоната на температурама изнад 825 ° Ц, што доводи до стварања вапна и угљен диоксида.
Горе наведена тврдња се може описати на следећи начин: ЦаЦО3(с) → ЦаО (с) + ЦО2(г) Зато што је земљина кора богата кречњаком и калцитом, ау океанима и плажама обилују морским шкољкама (сировине за производњу калцијум оксида), калцијум оксид је релативно јефтин реагенс.
Индек
- 1 Формула
- 2 Структура
- 3 Својства
- 3.1 Растворљивост
- 4 Усес
- 4.1 Као малтер
- 4.2 У производњи чаша
- 4.3 У рударству
- 4.4 Као средство за уклањање силиката
- 5 Наночестице калцијум оксида
- 6 Референце
Формула
Хемијска формула калцијум оксида је ЦаО, у којој је калцијум сличан киселинском јону (акцептор електрона) Ца2+, и кисеоник као базни јон (донор електрона) ОР2--.
Зашто калциј има +2 набоја? Будући да калцијум спада у групу 2 периодног система (г. Бецамбара), и има само два валентна електрона доступна за формирање веза, која даје атом кисеоника..
Структура
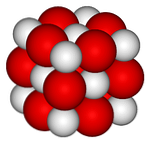
У горњој слици представљена је кристална структура (тип гем-соли) за калцијум-оксид. Волуминозне црвене сфере одговарају Ца јонима2+ и беле сфере до јона О2-.
У овом кубном кристалном распореду сваки јон Ца2+ је окружен са шест иона О2-, зачепљен у октаедарским рупама које остављају велики јони између њих.
Ова структура максимално изражава ионски карактер овог оксида, иако значајна разлика радијуса (црвена сфера је већа од беле) даје слабију кристалну ретикуларну енергију у поређењу са МгО.
Пропертиес
Физички, то је кристално бела чврста материја, без мириса и са јаким електростатичким интеракцијама, које су одговорне за високе тачке топљења (2572 ° Ц) и кључање (2850 ° Ц). Поред тога, има молекулску тежину од 55,958 г / мол и интересантно је да буде термолуминисцентан.
То значи да комад калцијум оксида који је изложен пламену може блистати интензивном белом светлошћу, познатом на енглеском језику са именом лимелигхт, или на шпанском, светлост калцијума. Иони Ца2+, у контакту са ватром, изазивају црвенкасти пламен, као што је приказано на сљедећој слици.

Растворљивост
ЦаО је основни оксид који има јак афинитет за воду, у мери у којој апсорбује влагу (она је хигроскопна чврста супстанца), реагујући одмах да производи гашени креч или калцијум хидроксид:
ЦаО (с) + Х2О (л) => Ца (ОХ)2(с)
Ова реакција је егзотермна (ослобађа топлоту) услед стварања чврсте супстанце са јачим интеракцијама и стабилнијом кристалном решетком. Међутим, реакција је реверзибилна ако се Ца (ОХ) загреје2, дехидрирање и паљење гашеног вапна; онда, лимета "се поново рађа".
Добијени раствор је веома базичан, а ако је засићен калцијум оксидом, он достигне пХ од 12,8.
Исто тако, раствара се у глицеролу иу киселим и шећерним растворима. Пошто је то основни оксид, он природно има ефективне интеракције са киселим оксидима (СиО2, Ал2О3 анд Фаитх2О3, на пример, растворљив у течној фази. С друге стране, он је нерастворљив у алкохолима и органским растварачима.
Усес
ЦаО има велики број индустријских намена, као и синтезу ацетилена (ЦХ≡ЦХ), у екстракцији фосфата из отпадних вода иу реакцији са сумпор диоксидом из гасовитог отпада..
Друге употребе калцијум оксида описане су у наставку:
Као минобацач
Ако се калцијум оксид помеша са песком (СиО2) и воду, пеците са песком и полако реагујете са водом да би формирали гашени креч. Заузврат, ЦО2 ваздуха се раствара у води и реагује са сољу како би се формирао калцијум карбонат:
Ца (ОХ)2(с) + ЦО2(г) => ЦаЦО3(с) + Х2О (л)
Тхе ЦаЦО3 То је отпорнија и тврђа смјеса од ЦаО, због чега морт (претходна смјеса) отврдњава и фиксира цигле, блокове или керамику између њих или на жељену површину..
У производњи чаша
Основна сировина за производњу стакла су оксиди силиција, који се мешају са кречом, натријум карбонатом (На2ЦО3) и других адитива, да би се затим подвргли загревању, што је резултирало стакластом чврстоћом. Ова чврста супстанца се затим загрева и упухује у било којој слици.
Ин мининг
Гашено вапно заузима већи волумен од вапна због интеракција водоничних веза (О-Х-О). Ово својство се користи за разбијање стијена изнутра.
То се постиже пуњењем компактном мјешавином вапна и воде, која је запечаћена да фокусира своју топлину и експанзивну снагу у стијени..
Као силикатни одстрањивач
ЦаО се спаја са силикатима да би се формирала коалесцентна течност, која се затим екстрахује из сировине одређеног производа..
На пример, руде гвожђа су сировина за производњу металног гвожђа и челика. Ови минерали садрже силикате, који су непожељне нечистоће у процесу и елиминишу се управо описаним поступком.
Наночестице калцијум оксида
Калцијум оксид се може синтетизовати као наночестице, варирајући концентрације калцијум нитрата (Ца (НО)3)2) и натријум хидроксид (НаОХ) у раствору.
Ове честице су сферичне, основне (као и макро-чврсте) и имају велику површину. Према томе, ова својства доприносе каталитичким процесима. Који? Истрага тренутно одговара на то питање.
Ове наночестице су коришћене за синтезу супституисаних органских једињења - изведених из пиридина - у формулацији нових лекова за спровођење хемијских трансформација као што је вештачка фотосинтеза, за пречишћавање воде од тешких и штетних метала, и фотокаталитички агенси.
Наночестице се могу синтетизовати на биолошкој подлози, као што су листови папаје и зеленог чаја, да би се користили као антибактеријски агенс..
Референце
- сцифун.орг (2018). Лиме: калцијум оксид. Преузето 30. марта 2018. године са: сцифун.орг.
- Википедиа. (2018). Калцијум оксид. Преузето 30. марта 2018. године са: ен.википедиа.орг
- Асхвини Анантхараман ет ал. (2016). Зелена синтеза наночестица калцијум оксида и њене примене. Инт. Јоурнал оф Енгинееринг Ресеарцх анд Апплицатион. ИССН: 2248-9622, Том 6, Издање 10, (Парт -1), стр. 27-31.
- Ј. Сафаеи-Гхоми ет ал. (2013). Наночестице калцијум оксида катализоване једностепеном вишекомпонентном синтезом високо супституисаних пиридина у воденој средини етанола Сциентиа Ираница, Трансацтионс Ц: Хемија и хемијско инжењерство 20 549-554.
- ПубЦхем. (2018). Калцијум оксид. Преузето 30. марта 2018. године, из: пубцхем.нцби.нлм.них.гов
- Схивер & Аткинс. (2008). Неорганска хемија Ин Елементи групе 2. (четврто издање, стр. 280). Мц Грав Хилл.


