Хемијска структура, својства и употреба амонијум-сулфата
Тхе амонијум сулфат То је тернарна и амонијачна неорганска со сумпорне киселине. Његова хемијска формула је (НХ.)4)2СО4. Према томе, стехиометријски проценти кажу да за сваки анион сулфата постоје два амонијумска катјона која су у интеракцији са њом. Ово омогућава неутралност соли ((+1) + 2 + (-2)).
Његова номенклатура је резултат чињенице да је то сол изведена из Х2СО4, мењање суфикса "уриц" на "ато". Дакле, два почетна протона су замењена са НХ4+, реакциони производ са амонијаком (НХ3). Затим, хемијска једначина за његову синтезу је: 2 НХ3 + Х2СО4 => (НХ4)2СО4
Амонијум сулфат је складиште азота и сумпора, и неопходно у хемији земљишта и ђубрива.
Индек
- 1 Хемијска структура
- 2 Физичка и хемијска својства
- 2.1 Молекуларна тежина
- 2.2 Физички изглед
- 2.3 Мирис
- 2.4 Тачка топљења
- 2.5 Растворљивост
- 2.6 Густина
- 2.7 Притисак паре
- 2.8 Пламиште
- 2.9 пХ
- 2.10 Стабилност
- 2.11 Декомпозиција
- 2.12 Корозија
- 3 Усес
- 3.1 У пољопривреди
- 3.2 Као аналитички реагенс
- 3.3 У таложењу и изолацији протеина
- 3.4 У индустрији
- 3.5 Друге употребе
- 4 Референце
Хемијска структура
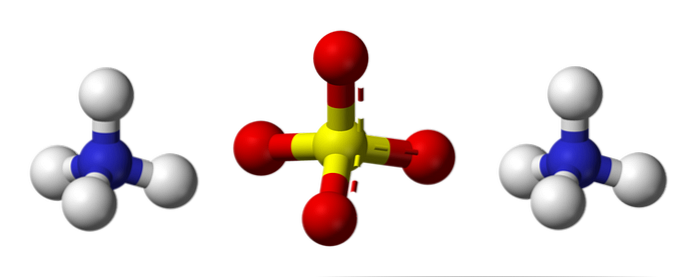
Горња слика илуструје геометрију молекула НХ јона4+ и СО42-. Црвене сфере одговарају атомима кисеоника, белим сферама одговарају атоми водоника, плаве сфере атому азота и жуте сфере одговарају атому сумпора..
Оба иона се могу сматрати два тетраедра, тако да имају три јединице које интерагују и формирају орторомбски кристални распоред. Сулфат анион је СО42- и способан је донирати или прихватити четири водикове везе, баш као и НХ катион4+.
Физичке и хемијске особине
Молекуларна тежина
132,134 г / мол.
Физички изглед
Солид вхите. Орторомбски бели или смеђи кристали, у зависности од нивоа нечистоћа.
Мирис
Тоалет.
Тачка топљења
280 ºЦ. Ова тачка топљења, ниска у поређењу са другим јонским једињењима, последица је чињенице да је то сол са моновалентним катионима (+1) и са различитим јонима у својим величинама, због чега чврста материја има ниску кристалну ретикуларну енергију..
Растворљивост
76.4 г / 100 г воде на 25 ° Ц. Овај афинитет за воду је због великог капацитета његових молекула за солватирање амонијумових јона. С друге стране, нерастворан је у ацетону и алкохолу; то јест, у растварачима који су мање поларни од воде.
Густина
1.77 г / цм3 на 25 ºЦ.
Притисак паре
1,871 кПа на 20 ºЦ.
Тачка запаљивости
26 ºЦ.
пХ
5,0-6,0 (25 ° Ц, 1 М раствор). Благо кисели пХ је резултат хидролизе НХ4+ у води, стварајући Х3О+ у ниским концентрацијама.
Стабилност
Стабилан у одговарајућим условима околине. У контакту са јаким оксидансима може се запалити.
Децомпоситион
Почиње да се распада на 150 ºЦ, ослобађајући токсичне паре сумпор оксида, азотног оксида и амонијака.
Корозија
Не напада гвожђе или алуминијум.
Усес

У пољопривреди
- Амонијум сулфат се користи као ђубриво у алкалним земљиштима. Амонијумова со у свом саставу има 21% азота и 24% сумпора. Међутим, постоје једињења која обезбеђују већу количину азота од амонијум сулфата; Предност потоњег је његова висока концентрација сумпора.
- Сумпор је неопходан у синтези протеина, пошто неколико аминокиселина - као што су цистин, метионин и цистеин - поседују сумпор. Из ових разлога, амонијум сулфат је и даље једно од најважнијих ђубрива.
- Користи се у усевима пшенице, кукуруза, пиринча, памука, кромпира, конопље и воћака.
- Низак пХ алкалних земљишта због њиховог доприноса процесу нитрификације микробима. Користи се амонијум (НХ)4+) за производњу нитрата (бр3-и ослободити Х+: 2НХ4+ + 4О2 => 2НО3- + 2Х2О + 4Х+. Повећање концентрације водоника смањује пХ алкалних земљишта и омогућава већу употребу.
- Осим што се користи као ђубриво, амонијум сулфат делује као коадјувант за растворљиве инсектициде, хербициде и фунгициде, који се прскају на усеве..
- Сулфат је способан да издвоји ионе присутне у земљишту и води за наводњавање која су неопходна за живот одређених патогена. Међу јонима које хвата амонијум сулфат су Ца2+, тхе Мг2+, Вера2+ и Вера3+. Ово дејство појачава микробицидно дејство поменутих агенаса.
Као аналитички реагенс
Амонијум сулфат делује као средство за таложење у електрохемијској анализи, у микробиолошким медијумима за културу и у припреми амонијумових соли.
У таложењу и изолацији протеина
Амонијум сулфат се користи у изолацији и пречишћавању протеина, посебно протеина плазме. Количина амонијум сулфата се додаје плазми до одређене концентрације; тако је изазвано таложење групе протеина.
Преципитат се сакупља центрифугирањем и додаје се додатна количина амонијум сулфата у супернатант и, при новој концентрацији, долази до таложења друге групе протеина..
Понављање претходног процеса у секвенцијалном облику омогућава добијање различитих фракција протеина плазме.
Пре него што су се појавиле нове технологије молекуларне биологије, ова процедура је омогућила изолацију протеина плазме од великог значаја у медицини, на пример: имуноглобулини, фактори коагулације итд..
У индустрији
Амонијум сулфат спречава почетак пожара у текстилној индустрији. Користи се као адитив у индустрији галванизације. Такође се користи у производњи водоник пероксида, амонијум хлорида, итд..
Отхер усес
- Амонијум сулфат се користи као средство за регулацију осмотског притиска и као средство за таложење соли.
- У облику амонијум лаурил сулфата, површинска напетост воде се смањује, чиме се омогућава одвајање загађивача повећањем тврдоће воде..
- То је антикорозивни агенс.
- Користи се као додатак храни који регулише киселост у брашно и хлеб.
Референце
- ОЕЦД СИДС. (Октобар 2004). Амонијум сулфат. [ПДФ] Преузето 27. априла 2018. године, од: инцхем.орг
- Компанија Мосаиц. (2018). Амонијум сулфат. Преузето 27. априла 2018. године из: цропнутритион.цом
- Википедиа. (2018). Амонијум сулфат. Преузето 27. априла 2018. године, са: ен.википедиа.орг
- Пубцхем. (2018). Амонијум сулфат. Преузето 27. априла 2018. године, од: пубцхем.нцби.нлм.них.гов УпСтицксНГо Црев.
- (23. јул 2015). [Фигуре] Преузето 27. априла 2018. године, са: флицкр.цом
- Паула Папп (22. фебруар 2017.). Примена и употреба амонијум сулфата. Преузето 27. априла 2018. године из: бусинесс.цом


