Алуминијум сулфат (Ал2 (СО4) 3) структура, употреба, типови, токсичност
Тхе алуминијум сулфат је неорганска алуминијумова со формуле Ал2(СО4)3, који се обично појављује као бела чврста маса са сјајним кристалима. На боју једињења утиче његова концентрација гвожђа и било које друге нечистоће. Постоје два главна типа алуминијум сулфата: А и Б.
На доњој слици приказани су бели кристали хидрираног алуминијум сулфата. Може се уочити одсуство смеђих обојења, што указује на ионе гвожђа унутар кристалне решетке.

Алуминијум сулфат је сол која је веома растворљива у води и по природи је ретка у анхидрованом облику. Обично се хидрира у облику октадекахидрата алуминијум сулфата [Ал2(СО4)3.18Х2О] или хексадекахидрат [Ал2(СО4)3.16Х2О].
Исто тако, он може да формира двоструке соли са калијумом, и са амонијумом, једињењима познатим као алумини. Делимично то може бити због афинитета воде у хидратима да задржи друге ионе осим алуминијума.
Алуминијум сулфат се може разградити дејством воде у алуминијум хидроксиду и сумпорној киселини. Ово својство је омогућило његову употребу као средство за закисељавање земљишта.
Такође је токсично једињење, нарочито контактом са прахом. Међутим, има бесконачност употребе и примена које иду од пречишћавања воде методом коагулације, која се одвија кроз његову употребу у неколико индустрија, до њене употребе са терапеутским циљевима..
Индек
- 1 Струцтуре
- 2 Шта је за (користи)
- 2.1 Коагулација или флокулација воде
- 2.2 Користити као жбуку мастила иу изради папира
- 2.3 Индустријска употреба
- 2.4 Лековите и терапеутске употребе
- 2.5 Друге употребе
- 3 Производња алуминијум сулфата
- 4 Типови
- 5 Токсичност
- 6 Референце
Структура
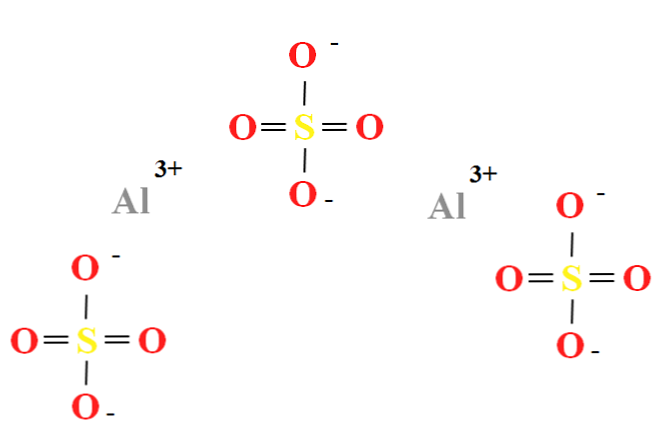
Алуминијум сулфат има однос два Ал катиона3+ за свака три аниона СО42- (горња слика), која се може посматрати директно у њеној хемијској формули Ал2(СО4)3.
Приметите да је Ал3+ они су сивкасти, док СО42- они су жути (за атом сумпора) и црвени (за атоме кисеоника).
Приказана структура одговара безводном облику Ал2(СО4)3, пошто ниједан молекул воде не ступа у интеракцију са јонима. Међутим, у вашим хидратима вода може бити привучена позитивним центрима Ал3+, или негативним СО тетраедром42- преко водоничних веза (ХОХ-О-СО32-).
Ал2(СО4)3Х 18Х2Или, на пример, садржи 18 молекула воде у својој чврстој структури. Неки од њих могу бити у директном контакту са Ал3+ или са СО42-. Другим речима: алуминијум сулфат може имати унутрашњу или спољашњу координациону воду.
Такође, његова структура може да прими друге катионе као што је Фе3+, На+, К+, итд. Али за то је неопходно присуство више аниона СО42-. За шта? Неутрализовати повећање позитивних набоја због металних нечистоћа.
Алуминијум сулфат може имати много структура, иако његови хидрати имају тенденцију да усвоје моноклински кристални систем.
Физичке и хемијске особине
Изглед
Изгледа као чврста супстанца са сјајним белим кристалима, гранулама или прахом.
Молекуларна тежина
342,31 г / мол (безводни).
Мирис
Без мириса је
Тасте
Слатки укус умјерено адстрингентан.
Тачка топљења
Анхидрована форма од 770º Ц (форма 86,5º Ц октадекахидратада)
Растворљивост у води
31.2 г / 100 мл на 0 ° Ц; 36.4 г / 100 мл на 20 ° Ц и 89 г / 100 мл на 100 ° Ц.
Густина
2,67 до 2,71 г / цм3.
Растворљивост
Слабо растворљив у етил алкохолу.
Притисак паре
У суштини нула.
Стабилност
Стабилан у ваздуху.
Децомпоситион
Када се загрева, приближно на тачки његовог топљења, може се разградити емитовањем посебно оксида сумпора, токсичног гаса.
Корозивност
Раствори алуминијум сулфата су корозивни за алуминијум. Такође, једињење може кородирати метале у присуству влаге.
пКа
3.3 до 3.6. Његов пХ је 2,9 или више у 5% воденом раствору.
Шта је за (користи)
Коагулација или флокулација воде
-Када се помеша са водом (питком, сервираном или отпадом), алуминијум сулфат изазива алуминијум хидроксид, који формира комплексе са једињењима и честице у раствору убрзавајући њихову седиментацију, која би у одсуству третмана са алуминијум сулфатом била потребна дуго времена.
-Алуминијум сулфат се такође користи за чишћење воде у базенима, што их чини привлачнијим за употребу.
-Коришћењем алуминијум сулфата, вода се добија без замућења и боје, чиме се повећава њена способност за поспешивање чишћења воде. Нажалост, овај начин пречишћавања може довести до незнатно повећане концентрације алуминијума у води.
-Алуминијум је веома токсичан метал који се накупља у кожи, мозгу и плућима, изазивајући озбиљне поремећаје. Осим тога, није познато која функција испуњава у живим бићима.
-Европска унија захтева да максимално дозвољена граница алуминијума у води не прелази 0,2 мг / л. У међувремену, Америчка агенција за заштиту животне средине захтева да максимална граница контаминације воде алуминијумом не прелази 0.05-0.2 мг / л.
-Третирање отпадних вода или употреба алуминијум сулфата омогућава економично уклањање или смањење фосфора у њима.
Користити као жбуку мастила иу изради папира
-Алуминијум сулфат је коришћен као средство за чишћење боја и мастила, помажући при фиксирању материјала који се боји. Његова акција фиксирања је због Ал (ОХ)3, чија желатинозна конзистенција доприноси адсорпцији боја на текстилу.
-Иако се за описану намену користи од 2000. године пре нове ере, само органске боје захтевају средства за испирање. Синтетичке боје, с друге стране, не захтевају монданте да би испуниле своју функцију.
-Замијењена је из производње папира, али се још увијек користи у производњи папирне пулпе. Уклања нечистоће, као и да се користи за везивање материјала, неутралише набоје и калибрише колофониј.
Индустријска употреба
-Користи се у грађевинарству како би се убрзало постављање бетона. Осим тога, користи се у хидроизолацији зграда.
-У индустрији сапуна и масти, користи се у производњи глицерина.
-Користи се у нафтној индустрији у производњи синтетичких катализатора који се користе током рада.
-Користи се у фармацеутској индустрији као адстригентно средство у припреми лијекова и козметике.
-Интервенише у производњи боја као што је кармин. Користи се и као боја за производњу синтетичких гума бутадиен стирена.
-У индустрији шећера користи се као прочишћивач меласе за шећерну трску.
-Користи се у производњи дезодоранса. Зашто? Зато што узрокује сужавање канала знојних жлезда, чиме се ограничава накупљање зноја, неопходан медијум за раст бактерија које узрокују мирис..
-Користи се у штављењу коже, што је неопходан процес за његову употребу. Осим тога, користи се у производњи ђубрива.
-Користи се као адитив у припреми боја, љепила и бртвила, као и производа за чишћење и његу намјештаја..
Медицинска и терапеутска употреба
-Алуминијум сулфат је имунолошки адјувант. Према томе, он испуњава функцију обраде антигена на такав начин да, када се ослободе на месту њиховог деловања, производе већу производњу антитела за антигене који су инокулисани.
-Фреундови адјуванти и БЦГ, као и други адјуванси, укључујући ендогене, као што су интерлеукини, су неспецифични за антигене, дозвољавајући повећање радијуса имуног дејства. То је омогућило развој вакцина против бројних болести.
-Коагулационо дејство алуминијум сулфата омогућило је елиминацију бројних вируса у третираној води, између осталих: К бета, МС2, Т4 и П1. Резултати указују да третман воде алуминијум сулфатом производи инактивацију таквих вируса.
-Алуминијум сулфат се користи у облику штапића или као прах у лечењу малих површинских рана или огреботина насталих приликом бријања.
-Користи се у производњи алуминијум ацетата, једињења које се користи у третману неких услова уха. Такође се користи, без значајног успеха, да се ублаже последице пожара..
-Употребљавају се раствори алуминијум сулфата, у концентрацији од 5% до 10%, у локалном третману чирева који омогућавају контролу њихових секрета.
-Адстрингентно дејство алуминијум сулфата контрахује површинске слојеве коже, коагулира протеине и зацјељује ране.
Отхер усес
-Алуминијум сулфат помаже у контроли прекомерног раста алги у рибњацима, језерима и водотоцима. Користи се и за уклањање мекушаца, између осталог и за шпанског пужева.
-Вртари примењују ово једињење да би закисели алкална тла. У контакту са водом, алуминијум сулфат се разлаже на алуминијум хидроксид и разблажену сумпорну киселину. Затим се алуминијум хидроксид таложи, остављајући сумпорну киселину у раствору.
-Закисељавање земљишта због сумпорне киселине се визуелизује на веома креативан начин, због постојања биљке која се зове Хортензија, чији цветови постају плави у присуству киселог земљишта; то јест, они су осјетљиви и реагирају на промјене пХ вриједности.
-Алуминијум сулфат је укључен у производњу пене за борбу и контролу пожара. Како? Реагује са натријум бикарбонатом, производећи ослобађање ЦО2. Овај гас блокира приступ2 на место сагоревања материјала; а тиме и прекид ватре који се развијао.
Производња алуминијум сулфата
Алуминијум сулфат се синтетизује реакцијом једињења богатог алуминијумом, као што је бокситна руда, са сумпорном киселином на повишеним температурама. Следећа хемијска једначина представља реакцију:
Ал2О3 + Х2СО4 -> Ал2(СО4)3 + 3 Х2О
Алуминијум сулфат се такође може формирати реакцијом неутрализације између алуминијум хидроксида и сумпорне киселине, према следећој реакцији:
2 Ал (ОХ)3 + 3 Х2СО4 + 12 Х2О -> Ал2(СО4)3.18Х2О
Сумпорна киселина реагује са алуминијумом у облику амонијум сулфата и ослобађање молекула водоника у облику гаса. Реакција је схематизована на следећи начин:
2 Ал + 3 Х2СО4 -> Ал2(СО4)3 + 3 Х2
Типови
Алуминијум сулфат се класификује у два типа: тип А и тип Б. У алуминијум сулфату типа А, чврсте материје су беле и имају концентрацију гвожђа мању од 0.5%.
У алуминијум сулфату типа Б, чврсте материје су браон и имају концентрацију гвожђа мању од 1,5%.
Постоје индустрије које производе алуминијум сулфат и имају различите критеријуме за њихову класификацију. Према томе, индустрија је извјештавала за припрему алуминијум сулфата типа А максималну концентрацију од 0,1% жељеза као жељезног оксида. Док за тип Б они указују на максималну концентрацију гвожђа од 0,35%.
Токсичност
-Алуминијум сулфат је једињење које испољава своје токсично дејство у контакту са својом прашином, изазивајући иритацију коже, ау случајевима када је контакт чест, дерматитис.
-У очима изазива јаку иритацију, чак и за трајне повреде.
-Удисање изазива иритацију носа и грла, што може изазвати кашаљ и осип.
-Његов унос узрокује иритацију желуца, мучнину и повраћање.
-Постоје токсични ефекти који, иако нису директно повезани са алуминијум сулфатом, индиректно су последица њихове употребе. То је случај са одређеним токсичним ефектима алуминијума узрокованим употребом алуминијум сулфата у пречишћавању воде.
-Пацијенти који су хронично дијализирани употребом соли припремљених у пречишћеној води, употребом алуминијум сулфата, доживљавају врло тешке здравствене поремећаје. Међу овим поремећајима имамо анемију, деменцију путем дијализе и повећање болести костију.
Референце
- Википедиа. (2018). Алуминијум сулфат Такен фром: ен.википедиа.орг
- Арис Индустриал Раствор алуминијум сулфата типа А и Б. Узето из: арис.цом.пе
- Цхристопхер Боид (9. јун 2014). Топ индустријска употреба за алуминијум сулфат. Преузето из: цхемсервице.цом
- ПубЦхем. (2018). Анхидровани алуминијум сулфат. Преузето из: пубцхем.нцби.нлм.них.гов
- Андесиа Цхемицалс (20. август 2009). Сигурносни лист алуминијум сулфата. [ПДФ] Такен фром: андесиа.цом
- Цхемицал Боок. (2017). Алуминијум сулфат. Преузето из: цхемицалбоок.цом


