Структура, својства, употреба, токсичност, натријум-хлорид (НаЦл)
Тхе натријум хлорид, који се називају и обичном соли или столном соли, је бинарна неорганска со натријума алкалног метала и халогеног хлора. То је највећа компонента јестиве соли и њена минерална форма је позната као халит. Његова молекуларна формула је НаЦл и описује стехиометријски однос његових јона (На+ Цл-) а не дискретни молекул (На-Цл)
Натријум-хлорид је кристална бела чврста супстанца која се формира комбинацијом натријума, сребрног белог метала, који бурно реагује са водом, а хлорни елемент, отровни, корозивни, бледозелени гас.

На горњој слици је приказан део кристала НаЦл. Како је могуће да су два елемента опасна као На и Цл2, Може ли се формирати јестива сол? Прво, хемијска једначина за њено формирање је:
2На (с) + Цл2(г) => 2НаЦл (с)
Одговор лежи у природи везе у НаЦл. Бити ионски, својства На+ и Цл- они су дијагонално различити од оних њихових неутралних атома.
Натријум је витални елемент, али у свом јонском облику. Тхе На+ је главни екстрацелуларни катион са концентрацијом од приближно 140 мЕк / лт, и заједно са својим пратећим ањонима, Цл- и ХЦО3- (бикарбонат), углавном су одговорни за вредност осмоларности и екстрацелуларне запремине.
Поред тога, На+ одговоран је за стварање и провођење нервних импулса у неуронским аксонима, као и за покретање мишићне контракције.
НаЦл се од давнина користи за окус хране и очување меса, због његове способности да елиминише бактерије и спречи кварење.
Такође је неопходно за производњу натријум хидроксида (НаОХ) и молекуларног хлора (Цл2), реаговањем НаЦл са водом под хидролизом:
2Х2О (л) + 2 НаЦл (с) => 2НаОХ (ац) + Цл2(г) + Х2(г)
У катоди (-) Х се акумулира2 (г) и НаОХ. У међувремену, Цл се акумулира на аноди (+)2 (г) Натријум хидроксид се користи у производњи сапуна и хлора у производњи ПВЦ пластике.
Индек
- 1 Структура натријум хлорида
- 1.1 Унитари целл
- 2 Својства
- 2.1 Молекуларна формула
- 2.2 Молекуларна тежина
- 2.3 Физички опис
- 2.4 Боја
- 2.5 Тасте
- 2.6 Тачка кључања
- 2.7 Тачка топљења
- 2.8 Растворљивост у води
- 2.9 Растворљивост у органским растварачима
- 2.10 Густина
- 2.11 Притисак паре
- 2.12 Стабилност
- 2.13 Декомпозиција
- 2.14 Вискозност
- 2.15 Корозија
- 2.16 пХ
- 3 Усес
- 3.1 У храни
- 3.2 Индустријска употреба
- 3.3 Код куће
- 3.4 Друге употребе
- 3.5 Терапијске употребе
- 4 Токсичност
- 4.1 Гутање
- 4.2 Иритација и физички контакт
- 5 Референце
Структура натријум хлорида
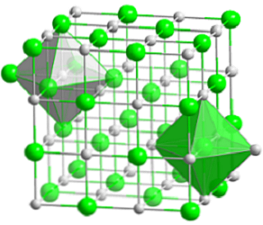
Компактна кубична структура натријум хлорида је представљена у горњој слици. Волуминозне зелене сфере одговарају Цл анионима-, док је бела, за На катионе+. Запазите како се кристал НаЦл састоји од мреже иона распоређених према њиховим електростатичким интеракцијама у односу 1: 1.
Иако су шипке приказане на слици, везе нису ковалентне већ ионске. Употреба шипки је корисна када се приказује координациона геометрија око јона. На пример, у случају НаЦл, сваки На+ окружен је са шест Цл- (бели октаедрон), и сваки Цл- од шест На+ (зелени октаедар).
Према томе, он има координацију (6,6) чији бројеви указују на то колико комшија окружује сваки ион. Број на десној страни означава сусједе На+, док је онај са леве стране, Цл-.
Други прикази изостављају употребу шипки за осветљавање октаедарних рупа које структура има, што је резултат интерстицијског простора између шест Цл аниона.- (или На катиони+) пацкагед. Овај аранжман је уочен код других моно (МКС) или полиатомских неорганских соли и назива се гем со..
Унитари целл
Јединична ћелија камене соли је кубична, али које коцке то тачно представљају на слици изнад? Октаедри дају одговор. Оба покривају укупно четири мале коцке.
Ове коцке имају делове јона у својим врховима, ивицама и лицима. Пажљиво посматрање, јона На+ налази се у средини и дванаест на ивицама. Ион на једној ивици може да се дели са четири коцке. Дакле, постоје 4 На јона+ (12 × 1/4 + 1 = 4).
За јоне Цл-, осам се налазе у врховима и шест у рубовима. Како јони позиционирани на врховима дијеле простор са осам других коцки, а на рубовима са шест, имају 4 Цл ионе- (8 × 1/8 + 6 × 1/2 = 4).
Претходни резултат се тумачи на следећи начин: у јединичној ћелији НаЦл постоје четири На катиона+ и четири Цл аниона-; пропорција која одговара хемијској формули (На+ за сваки Цл-).
Пропертиес
Молекуларна формула
НаЦл.
Молекуларна тежина
58.44 г / мол.
Физички опис
Кристална чврста супстанца.
Боја
Прозирни безбојни кристали или бели кристални прах.
Тасте
Салти.
Тачка кључања
2.575 ºФ до 760 ммХг.
1,465 ºЦ.
Тачка топљења
1,474 ºФ (800,7 ºЦ).
И тачка кључања и тачка топљења одражавају топлоту потребну за превазилажење кристалне ретикуларне енергије. Према томе, ова мерења потврђују јонски карактер НаЦл.
Растворљивост у води
Већа или једнака 100 мг / мл на 68 ° Ф.
36.0 г / 100 мл на 25 ° Ц.
То је заправо хигроскопна со, која задржава влагу из околине.
Растворљивост у органским растварачима
0.065 г / 100 мЛ етанола на 25 ° Ц; 10 г / 100 г глицерола на 25 ° Ц; 2.15 г / 100 мЛ течног амонијака на 40 ° Ц; 1.4 г / 100 мЛ метанола на 25 ° Ц; 7.15 г / 100 етилен гликола на 25 ° Ц и 5.21 г / 100 г мравље киселине на 25 ° Ц.
Густина
2,165 г / цм3 на 77 ºЦ.
Притисак паре
1 ммХг до 1,589 ºФ.
Стабилност
Стабилан је под препорученим условима складиштења.
Децомпоситион
Када се загреје до високих температура, разграђује емитовање пара хлороводоничне киселине и динатријум оксида.
Вискозност
Вискозност засићених раствора 1.93 мПа-с.
Корозија
Корозивно је за многе метале.
пХ
6.7 до 7.3 у воденом раствору.
Усес
У храни
-Натријум-хлорид се од давнина користи за побољшање укуса хране и њеног очувања. Сољење меса је начин његовог очувања од бактеријске активности, јер одлаже разградњу протеина.
-С друге стране, сол повећава осмоларност око меса, што узрокује апсорпцију осмозом воде бактерија која узрокује његову елиминацију..
Индустријска употреба
Прехрамбена индустрија
-У прехрамбеној индустрији, сол се користи као појачивач окуса, адитив за контролу ферментације, средство за контролу текстуре и девелопер боје. На пример, додаје се со како би се истакла боја у сланини, шунци и другим месним производима.
-Сол служи као везиво у производњи кобасица. Она доприноси формирању везивног гела састављеног од меса, масти и влаге.
-Приликом прераде брашна за прављење хлеба додаје се со у току кувања ради контроле брзине ферментације теста. Користи се и за јачање глутена и појачивача укуса, као и за пуњење печених производа.
-Користи се у производњи житарица за доручак, мешаних или припремљених брашна, помфрита, јела за псе и мачке итд..
Синтеза хемијских производа
-Натријум-хлорид се користи као сировина у производњи натријум-хидроксида и хлора, што је корисно у многим хемијским индустријама.
-Сол се користи у обради различитих метала, на пример алуминијума, бакра, челика и ванадијума. Користи се и за прављење натријум хлората, који се касније користи у синтези хлор-диоксида, бјелила на бази кисеоника. Хлор диоксид је мање штетан за околину него други избјељивачи.
У индустрији коже
-Сол се користи за инхибицију бактеријске активности унутар коже, као и за помоћ у њеној рехидрацији.
У текстилној индустрији
-Сол се користи као средство за бојање тканина. Користи се као средство за испирање слане воде за уклањање органских загађивача и за стварање позитивног набоја на површини тканина који омогућава спајање негативно наелектрисаних боја.
У нафтној индустрији
-У истраживању нафте и гаса, сол је важна компонента у бушотинама за бушење. Користи се за флокулацију и повећање густине бушотинских флуида, што омогућава превазилажење високог притиска гаса у бушотинама које треба постићи. Поред тога, сол одржава засићеност течности за бушење.
-Со помаже у сабијању земљишта на којем су изграђени путеви. Смањује померање узроковано у подземљу промјенама влаге и аутомобилског саобраћаја.
Код куће
Сол је коришћена при трљању за чишћење површина, лонаца и лонаца. Такође у превенцији плијесни и као средство за уклањање мрља. Такође се користи у многим брендовима шампона и пасти за зубе.
Отхер усес
На путевима
-У очекивању снежних путева путеви су прекривени сланом водом, што спречава спајање леда на површину пута. За одмрзавање се користи мешавина саламуре и соли, а понекад се додају и друге хемијске компоненте као што су магнезијум или хлориди калцијума. Употреба соли и слане воде није ефикасна на температурама испод -10ºЦ.
Приликом додавања соли долази до смањења криоскопске тачке, колигативног својства раствора, што на неки начин омета формирање леда..
-Због свог хигроскопног стања, сол се користи као јефтино средство за сушење.
У смолама које се користе за омекшавање воде
Тврда вода садржи јоне калцијума и магнезијума који ометају рад сапуна и производе наслаге алкалних материјала у различитим уређајима и цевима. У омекшавању воде користе се смоле за јоноизмењивање. Сол се користи у припреми и регенерацији смола.
На апаратима за гашење пожара
Натријум-хлорид се користи у апаратима за гашење пожара у борби против пожара у којима су присутни запаљиви метали, као што су магнезијум, калијум, натријум и легуре НК.
Сол делује као хладњак и такође као дробилица која ограничава приступ кисеоника на ватру.
У наочарима
Кристали натријум хлорида се користе у оптичким компонентама као што су прозори и призме, посебно за инфрацрвено светло. Међутим, пошто је со веома хигроскопна, јавља се врста мраза који прекрива сочива. Због тога су сочива натријум хлорида замењена сочивима цинковог селенида (ЗнСе)..
Терапијска употреба
Да допуни недостатак соли у телу
-Када је тело осиромашено На+, Морају се заменити да би се одржао ванћелијски осмоларитет, нервна проводљивост и контракција мишића.
-НаЦл се користи у лечењу и превенцији недостатка натријума и хлора, што је последица прекомерног знојења током излагања високим температурама. Користи се и код прекомерне диурезе или претјераног ограничења уноса соли.
-Парентерална примена 045% раствора НаЦл се користи у лечењу хиперосмоларног дијабетеса. Испуњава рехидратациону функцију и служи за процену стања бубрежне функције.
-Ињекције хипертоничних раствора, са концентрацијом НаЦл већом од 0.9% в / в,
-Користе се када постоји озбиљно осиромашење На+, као рестаурација есенцијалног иона. Ова хипонатријемија може бити последица третмана са слободним електролитима или концентрацијом На+.
Хипонатријемија може бити узрокована и прекомјерним уносом воде, а не контролом неадекватне функције бубрега.
У третманима и неконвенционалним употребама
-НаЦл раствори за инхалацију се користе за разблаживање лекова који се користе током процеса небулизације. Користи се и за прање и наводњавање трахеје. 0.9% слан раствор који се користи у назалним спрејевима.
-За интра-амнионску трансабдоминалну инсталацију користе се 20% раствори НаЦл, што доводи до касног побачаја током другог триместра трудноће.
-Натријум хлорид се може користити као локални антисептик. Захваљујући свом осмотском капацитету може дехидрирати широк спектар вируса и бактерија у неизгореном стању; стога се користи као болан антисептик за дезинфекцију рана.
Токсичност
Гутање
Има само штетан утицај на здравље ако је унос висок и дуго времена. Под овим околностима би се појавила хипернатремија са посљедичним повећањем екстрацелуларног волумена који би довео до високог крвног притиска.
Иритација и физички контакт
Има токсично дејство само ако је инхалација веома висока. У контакту са кожом у претераној форми може изазвати сувоћу. На крају, она изазива тренутну иритацију при контакту са очима.
Референце
- Схивер & Аткинс. (2008). Неорганска хемија (Четврто издање, стр. 84, 90, 93, 263). Мц Грав Хилл.
- Вхиттен, Давис, Пецк & Станлеи. Цхемистри (8. изд.). ЦЕНГАГЕ Леарнинг, стр. 482-483.
- Натријум хлорид (2018). Натријум хлорид: предности, користи, својства, ризици. Преузето са: цлоруродесодио.орг
- ПубЦхем. (2018). Натријум хлорид. Преузето са: пубцхем.нцби.нлм.них.гов
- Википедиа. (2018). Натријум хлорид. Такен фром: ен.википедиа.орг
- Америцан Елементс. (2018). Натријум хлорид. Преузето из: америцанелементс.цом


