Бутино структура, својства и употреба
Тхе бутино је хемијско једињење које припада групи алкина, карактерисано углавном имајући у својој структури најмање троструку везу између два атома угљеника.
Када се ради о утврђивању правила за назив алкина, ИУПАЦ (акроним на енглеском језику за Интернатионал Унион оф Пуре анд Апплиед Цхемистри) је утврдио да се користе исти као и за алкенес.

Основна разлика између номенклатуре обе врсте супстанци је у томе што је суфикс -он промењен на -или када се ради о једињењима која имају троструке везе у својој структури.
С друге стране, бутино се састоји само од угљика и водика, и долази у два облика: 1-бутин, који је у плиновитој фази под стандардним увјетима тлака и температуре (1 атм, 25 ° Ц); и 2-бутино, који је врста течне фазе произведене хемијском синтезом.
Индек
- 1 Хемијска структура
- 1.1 1-бутино
- 1.2 2-бутин
- 2 Својства
- 3 Усес
- 4 Референце
Хемијска структура
У молекулу познатом као бутино приказан је феномен структурне изомеризације положаја, који се састоји од присуства истих функционалних група у оба једињења, али сваки од њих је на другом месту ланца.
У овом случају, оба облика бутина имају идентичну молекулску формулу; међутим, у 1-бутину трострука веза се налази у угљенику број један, док се у 2-бутину налази у броју два. Ово их претвара у изомере положаја.
Због положаја троструке везе у једном од терминала 1-бутин структуре, сматра се терминалним алкином, док му међуположај троструке везе у 2-бутин структури даје класификацију интерног алкина..
Према томе, веза може бити само између првог и другог угљеника (1-бутин) или између другог и трећег угљеника (2-бутин). Ово је због примењене номенклатуре, где ће најнижа могућа нумерација увек бити дата позицији троструке обвезнице.
1-бутино
Једињење које се назива 1-бутин је такође познато као етилацетилен, због његове структуре и начина на који су његова четири угљеникова атома распоређена и везана. Међутим, када говоримо о томе бутино упућује се само на ову хемијску врсту.
У овом молекулу, трострука веза се налази у терминалном угљенику, што омогућава доступност атома водоника који дају велику реактивност.
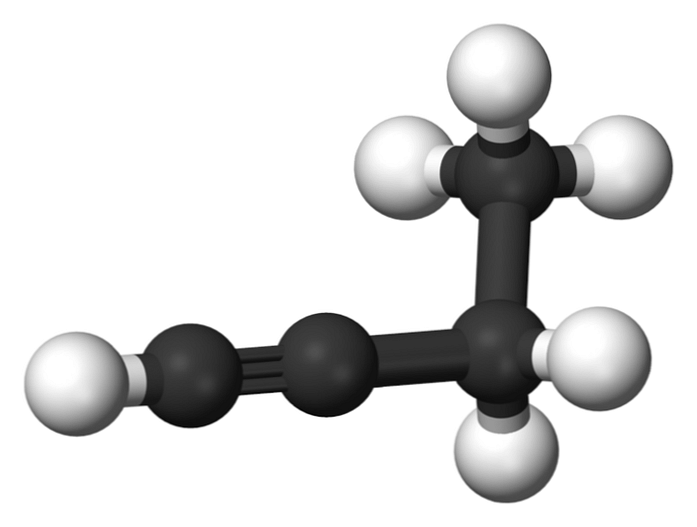
Ова крута и јача веза од једноструке или двоструке везе између атома угљеника обезбеђује стабилну конфигурацију 1-бутин линеарне геометрије.
С друге стране, ова гасовита супстанца је прилично запаљива, тако да у присуству топлоте може лако да изазове пожаре или експлозије и има велику реактивност у присуству ваздуха или воде..
2-бутине
Пошто интерни алкини показују већу стабилност од терминалних алкина, они дозвољавају трансформацију 1-бутина у 2-бутин.
Ова изомеризација се може десити загревањем 1-бутина у присуству базе (као што је НаОХ, КОХ, НаОЦХ3 ...) или преуређењем 1-бутина у раствору калијум хидроксида (КОХ) у етанолу (Ц).2Х6О).
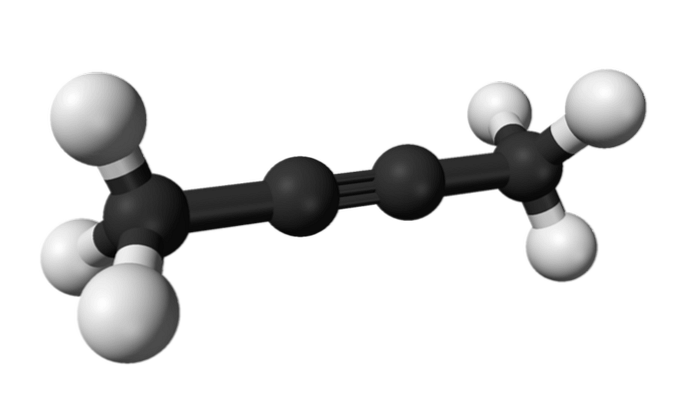
На исти начин, хемикалија позната као 2-бутин се назива и диметилацетилен (или кротонилен), представљајући се као течна и испарљива врста која настаје на вештачки начин.
У 2-бутину, трострука веза је у средини молекула, дајући јој већу стабилност од његовог изомера.
Поред тога, ово безбојно једињење има мању густину од воде иако се сматра нетопљивом у њему и има високу запаљивост.
Пропертиес
-Структурна формула бутина (без обзира на то који је изомер наведен) је Ц4Х6, која има линеарну структуру.
-Једна од хемијских реакција коју изазива бутилни молекул је изомеризација, у којој се у молекулу одвија прерасподела и миграција троструке везе..
-1-Бутин је у гасној фази, има веома високу запаљивост и већу густину од ваздуха.
-Ова супстанца је такође прилично реактивна и у присуству топлоте може изазвати насилне експлозије.
-Поред тога, када овај безбојни гас доживи непотпуну реакцију сагоревања може изазвати угљен моноксид (ЦО)
-Када су оба изомера изложена високим температурама, могу се појавити реакције полимеризације експлозивног типа.
-2-бутин се налази у течној фази, иако се сматра да је прилично запаљив под стандардним условима притиска и температуре.
-Ове супстанце могу имати јаке реакције када су у присуству јаких оксидационих супстанци.
-На исти начин, егзотермне реакције са последичним ослобађањем гасовитог водоника настају у присуству редуктивних врста..
-Када се нађу у контакту са одређеним катализаторима (као што су неке киселе супстанце) или почетне врсте, могу се појавити егзотермне реакције полимеризације.
Усес
Пошто имају нека друга својства, оба изомера могу имати различите употребе и примене, као што је приказано испод:
На првом месту, веома често једна од примена 1-бутина је његова употреба као средња фаза у процесу производње других супстанци органске природе синтетичког порекла..
С друге стране, ова хемијска врста се користи у прерађивачкој индустрији гуме и деривата; као на пример, када желите да добијете бензол.
Слично томе, користи се у процесу производње широког спектра пластичних производа, као иу производњи многих полиетиленских супстанци које се сматрају високом густином..
Такође, 1-бутин се често користи као компонента за процесе сечења и заваривања неких легура метала, укључујући челик (легура гвожђа и угљеник)..
У другом смислу, 2-бутин изомер се користи у комбинацији са другим алкином званим пропин у синтези неких супстанци познатих као алкилирани хидрохинони, када се одвија процес тоталне синтезе а-токоферола (витамина Е)..
Референце
- Википедиа. (с.ф.). Бутине Преузето са ен.википедиа.орг
- Иодер, Ц.Х., Лебер П.А. и Тхомсен, М.В. (2010). Мост до органске хемије: концепти и номенклатура. Преузето са боокс.гоогле.цо.ве
- Студи.цом. (с.ф.). Бутине: Струцтурал Формула & Исомерс. Добија се из студије.
- ПубЦхем. (с.ф.). 1-Бутине. Преузето са пубцхем.нцби.нлм.них.гов
- ПубЦхем. (с.ф.). 2-Бутине. Преузето са пубцхем.нцби.нлм.них.гов


