Атомски волумен како се мијења у периодичној табели и примјерима
Тхе атомска запремина је релативна вредност која указује на однос између моларне масе елемента и његове густине. Дакле, ова запремина зависи од густине елемента, а густина зависи, наизменично, од фазе и од тога како су атоми распоређени у овој фази..
Дакле, атомска запремина З елемента није иста у другој фази која се разликује од оне која показује на собној температури (течна, чврста или гасна), или када је део одређених једињења. Према томе, атомски волумен З у једињењу ЗА је различит од оног З у једињењу ЗБ.

Зашто? Да би га разумели, потребно је упоредити атоме са, на пример, мермерима. Кликови, попут плавичастих боја супериорне слике, веома добро су дефинисали своју материјалну границу, која се посматра захваљујући својој сјајној површини. Насупрот томе, граница атома је дифузна, мада се може сматрати удаљеном сферном.
Дакле, оно што одређује тачку изван граница атома је нулта вероватноћа проналажења електрона, и та тачка може бити даље или ближе нуклеусу у зависности од тога колико суседних атома интерагује око разматраног атома..
Индек
- 1 Атомска запремина и радијус
- 2 Додатна формула
- 3 Како се атомски волумен разликује у периодном систему?
- 3.1 Атомске запремине прелазних метала
- 4 Примери
- 4.1 Пример 1
- 4.2 Пример 2
- 5 Референце
Атомски волумен и радијус
Интеракцијом два Х-атома у Х молекули2, дефинисани су положаји њихових језгара, као и удаљености између њих (интернуклеарне удаљености). Ако су оба атома сферна, полупречник је растојање између језгра и дифузне границе:
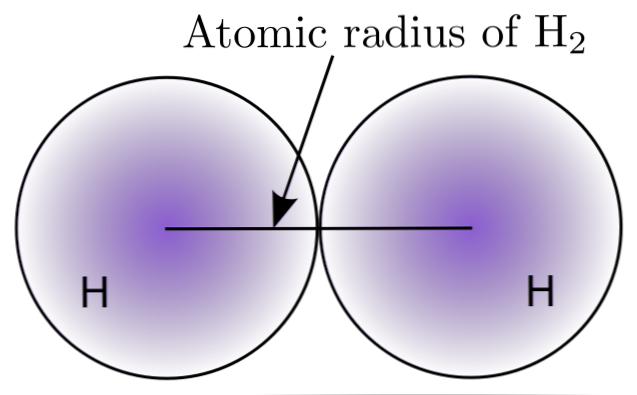
На горњој слици се види како се вјероватноћа проналажења електрона смањује како се удаљава од језгра. Поделом интернуклеарног растојања између два, добија се атомски полупречник. Затим, претпостављајући сферичну геометрију атома, користимо формулу за израчунавање запремине сфере:
В = (4/3) (Пи) р3
У овом изразу р је атомски радијус одређен за Х молекулу2. Вредност В израчуната овом непрецизном методом може да се промени ако се, на пример, сматра Х2 у течном или металном стању. Међутим, овај метод је веома нетачан јер су облици атома далеко од идеалне сфере у њиховим интеракцијама.
Да би се одредили атомски волумени у чврстим материјама, узимају се у обзир многе варијабле које се тичу распореда, и оне се добијају рендгенским дифракцијским студијама..
Додатна формула
Моларна маса изражава количину материје која има један мол атома хемијског елемента.
Његове јединице су г / мол. С друге стране, густина је волумен који заузима један грам елемента: г / мЛ. Пошто су јединице атомске запремине мл / мол, морате се играти са променљивим да би дошли до жељених јединица:
(г / мол) (мЛ / г) = мЛ / мол
Или шта је исто:
(Моларна маса) (1 / Д) = В
(Моларна маса / Д) = В
Тако се лако може израчунати запремина једног мола атома неког елемента; док је са сферном запремином израчуната запремина појединачног атома. Да би дошли до ове вредности од првог, неопходна је конверзија преко Авогадровог броја (6.02 · 10).-23).
Како се атомски волумен разликује у периодном систему?
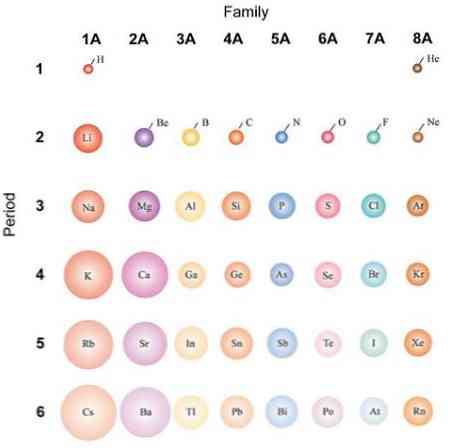
Ако се атоми сматрају сферичним, онда ће њихова варијација бити иста као и код атомских полупречника. На горњој слици, која показује репрезентативне елементе, илустровано је да се са десне стране остављају атоми патуљци; Уместо тога, од врха до дна постају све обимнији.
То је зато што у истом периоду нуклеус укључује протоне док се креће удесно. Ови протони испољавају атрактивну силу на спољне електроне, који осећају ефективно нуклеарно наелектрисање Зеф, мање од стварног нуклеарног набоја З.
Електрони унутрашњих слојева одбијају оне спољашњег слоја, смањујући ефекат језгра на њих; Ово је познато као ефекат екрана. У истом периоду ефекат екрана не успева да се супротстави повећању броја протона, тако да електрони у унутрашњем слоју не спречавају контракцију атома..
Међутим, спуштањем у групу, омогућени су нови нивои енергије, који омогућавају електронима да орбитирају даље од језгра. Такође, повећава се број електрона у унутрашњем слоју, чији заштитни ефекти почињу да се смањују ако нуклеус поново дода протоне..
Из ових разлога може се видети да група 1А има највише волуминозних атома, за разлику од малих атома групе 8А (или 18), од племенитих гасова..
Атомске запремине прелазних метала
Атоми прелазних метала укључују електроне у унутрашње орбите д. Ово повећање ефекта екрана и, као и стварног нуклеарног набоја З, поништавају се скоро једнако, тако да њихови атоми задржавају своју сличну величину у истом периоду..
Другим речима: у једном периоду прелазни метали показују сличне атомске запремине. Међутим, ове мале разлике су енормно значајне када се дефинишу метални кристали (као да су метални мермери).
Примери
Доступне су две математичке формуле за израчунавање атомске запремине елемента, свака са својим одговарајућим примерима.
Пример 1
С обзиром на атомски радијус водоника -37 пм (1 пицометар = 10-12м) - и цезијум -265 пм-, израчунати његове атомске запремине.
Користећи формулу сферног волумена, онда имамо:
ВХ= (4/3) (3.14) (37 пм)3= 212.07 пм3
ВЦс= (4/3) (3.14) (265 пм)3= 77912297,67 пм3
Међутим, ови волумени изражени у пирометрима су прекомјерни, па се претварају у јединице ангстрома, помножавајући их са конверзијским фактором (1А / 100пм)3:
(212.07 пм3) (1А / 100пм)3= 2.1207 × 10-4 А3
(77912297,67 пм3) (1А / 100пм)3= 77,912 А3
Дакле, разлике у величини између малог атома Х и гломазног атома Цс остају бројчано очигледне. Мора се имати на уму да су ови прорачуни само апроксимације под тврдњом да је атом потпуно кугласт, што лута у лице стварности.
Пример 2

Густина чистог злата је 19,32 г / мл, а њена моларна маса је 196,97 г / мол. Примена формуле М / Д за израчунавање запремине једног мола атома злата је следећа:
ВАу= (196.97 г / мол) / (19.32 г / мЛ) = 10.19 мЛ / мол
То јест, да 1 мол златних атома заузима 10.19 мЛ, али који волумен специфично заузима атом злата? И како то изразити у јединицама пм3? За ово једноставно примените следеће факторе конверзије:
(10.19 мЛ / мол) · (мол / 6.02 · 10)-23 атома) · (1 м / 100 цм)3· (13:00 / 10-12м)3= 16,92 · 106 пм3
Са друге стране, атомски радијус злата је 166 пм. Ако упоредите оба волумена - ону добијену претходном методом и ону која је израчуната помоћу формуле сферног волумена - наћи ћете да немају исту вредност:
ВАу= (4/3) (3.14) (166 пм)3= 19.15 · 106 пм3
Која је од та два најближа прихваћеној вриједности? Оно што је најближе експерименталним резултатима добијеним рендгенском дифракцијом кристалне структуре злата.
Референце
- Хелменстине, Анне Марие, Пх.Д. (9. децембар 2017.) \ Т. Атомиц Волуме Дефинитион. Преузето 6. јуна 2018. године из: тхоугхтцо.цом
- Маифаир, Андрев. (13. март 2018.) \ Т. Како израчунати јачину Атома. Сциенцинг. Преузето 6. јуна 2018. године из: сциенцинг.цом
- Вики Кидс Лтд. (2018). Лотхар Меиер Атомиц Волуме Цурвес. Преузето 6. јуна 2018. године, из: вондервхизкидс.цом
- Лумен Периодни трендови: атомски радијус. Преузето 6. јуна 2018. године, са: цоурсес.луменлеарнинг.цом
- Цамило Ј. Дерпицх. Запремина и атомска густина. Преузето 6. јуна 2018. године, са адресе: ес-пуракуимица.веебли.цом
- Вхиттен, Давис, Пецк & Станлеи. Цхемистри (8. изд.). ЦЕНГАГЕ Леарнинг, стр. 222-224.
- Фондација ЦК-12. (22. фебруар 2010). Упоредне величине атома. [Фигуре] Преузето 6. јуна 2018. године, са: цоммонс.викимедиа.орг
- Фондација ЦК-12. (22. фебруар 2010). Атомски радијус Х2. [Фигуре] Преузето 6. јуна 2018. године, са: цоммонс.викимедиа.орг


