Атомски радијус како се мјери, како се мијења у периодном систему, примјери
Тхе атомски радијус то је важан параметар за периодична својства елемената периодне табеле. То је директно повезано са величином атома, будући да су на већем радијусу већи или гломазнији. Исто тако, то се односи и на електронске карактеристике исте.
Све док атом има више електрона, већа је његова величина и атомски полупречник. Оба су дефинисана електронима валентне љуске, јер се на растојањима изван њихових орбита вероватноћа проналажења електрона приближава нули. Супротно од нуклеуса јавља се супротно: вероватноћа проналажења електрона се повећава.

Горња слика представља паковање памучних куглица. Имајте на уму да је сваки окружен са шест сусједа, без бројања другог могућег горњег или доњег реда. Начин на који се врећице памука збијају ће дефинисати њихове величине и, самим тим, њихове радијусе; као што се дешава са атомима.
Елементи у складу са њиховом хемијском природом међусобно делују са својим атомима на овај или онај начин. Према томе, величина атомског радијуса варира према типу присутне везе и чврстом паковању његових атома.
Индек
- 1 Како се мери атомски радијус?
- 1.1 Одређивање интернуклеарне удаљености
- 1.2 Унитс
- 2 Како се мијења периодни сустав?
- 2.1 Током периода
- 2.2 Спуштање групе
- 2.3 Контракција лантанида
- 3 Примери
- 4 Референце
Како се мери атомски радијус?
На главној слици може се лако измерити пречник лоптица од памука, а затим га поделити на два. Међутим, сфера атома није у потпуности дефинисана. Зашто? Зато што електрони циркулишу и дифундирају у специфичним просторима простора: орбитале.
Дакле, атом се може посматрати као сфера са непрепустивим ивицама, што је немогуће са сигурношћу рећи у којој мери се оне завршавају. На пример, у горњој слици средина региона, близу језгра, изгледа интензивније, а ивице су јој замућене..
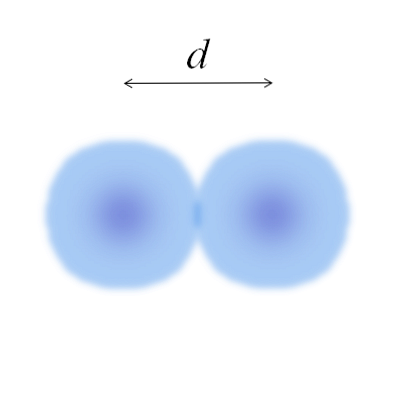
Слика представља двоатомски молекул Е2 (као Цл2, Х2, О2, итд.). Под претпоставком да су атоми сферна тела, ако је удаљеност одређена д која раздваја оба језгра у ковалентној вези, онда би било довољно да се подели на две половине (д2) да се добије атомски полупречник; прецизније, ковалентни радијус Е за Е2.
А ако Е не формира ковалентне везе са самим собом, већ је то метални елемент? Онда д на то би указивао број суседа који окружују Е у својој металној структури; то јест, координационим бројем (НЦ) атома у паковању (запамтите памучне куглице главне слике).
Одређивање интернуклеарне удаљености
Да одредим д, што је интернуклеарна дистанца за два атома у молекулу или паковању, то захтева технике физичке анализе.
Једна од најчешће коришћених је дифракција рендгенских зрака, у којој се зраке свјетлости обасјава кроз кристал и проучава се дифракцијски узорак који је резултат интеракције електрона и електромагнетног зрачења. У зависности од паковања, могу се добити различити дифракцијски обрасци и, према томе, друге вредности д.
Ако су атоми "чврсти" у кристалној решетки, они ће представљати различите вредности д у поређењу са оним што би имали да су "удобни". Такође, ове интернуклеарне удаљености могу осциловати у вредностима, тако да се атомски радијус заправо састоји од просечне вредности таквих мерења..
Како су повезани атомски радијус и координациони број? В. Голдсцхмидт је успоставио везу између ове две, у којој је за НП од 12 релативна вредност 1; од 0.97 за паковање где атом има Н.Ц једнако 8; од 0,96, за НЦ једнако 6; и 0,88 за НЦ од 4.
Јединице
Из вредности за Н.Ц једнако 12, конструисано је много табела у којима се упоређују атомски полупречници свих елемената периодне табеле..
Пошто сви елементи не формирају такве компактне структуре (НЦ мање од 12), однос В. Голдсцхмидт се користи за израчунавање њихових атомских радијуса и њихово изражавање за исто паковање. На овај начин, мерења атомских радијуса су стандардизована.
Али у којим јединицама се изражавају? Од д је веома мале величине, треба да се приближи ангстромским јединицама А (10. 10-10м) или такође широко коришћени пикометар (10. 10-12м).
Како се она мења у периодном систему?
Током периода
Атомски радијуси одређени за металне елементе добијају назив метални радијуси, док за оне неметалне елементе, ковалентне радијусе (као што је фосфор, П)4, или сумпор, С8). Међутим, између оба типа радија постоји израженија разлика од имена.
Од лева на десно у истом периоду, нуклеус додаје протоне и електроне, али су последњи ограничени на исти ниво енергије (главни квантни број). Као последица тога, нуклеус испољава повећање ефективног нуклеарног набоја на валентне електроне, који контрахују атомски полупречник.
На овај начин, неметални елементи у истом периоду имају тенденцију да имају атомске (ковалентне) радијусе мање од метала (метални радијуси).
Спуштање групе
Када се група спушта, омогућавају се нови нивои енергије, што омогућава електронима да имају више простора. Дакле, електронски облак покрива веће удаљености, његова замућена периферија завршава се удаљавањем од нуклеуса, и самим тим, атомски полупречник се шири.
Лантанидне контракције
Електрони унутрашњег слоја помажу да се штити ефективно нуклеарно наелектрисање од валентних електрона. Када орбитале које сачињавају унутрашње слојеве имају много "рупа" (чворова), као и код ф орбитала, језгро снажно контрахује атомски радијус због лошег ефекта заштите орбитала..
Ова чињеница је доказана у контракцији лантанида у периоду 6 периодне табеле. Од Ла до Хф постоји значајна контракција атомског полупречника произведеног орбиталима ф, који "попуњавају" како пролази кроз блок ф: онај од лантханоида и актиноида.
Сличан ефекат се може приметити и код елемената блока п из периода 4. Овај временски производ слабог заштитног ефекта орбитала д који се попуњавају при укрштању периода прелазних метала.
Примери
За период 2 периодне табеле атомски радијуси његових елемената су:
-Ли: 257 пм
-Будите: 112 сати
-Б: 88 сати
-Ц: 77 пм
-Н: 74 пм
-О: 66 сати
-Ф: 64 п.м.
Треба напоменути да литијумски метал има највећи атомски радијус (257 п.м.), док је флуор, који се налази на крајњем десном делу периода, најмањи од њих (64 часа). Атомски радијус се спушта с лева на десно у истом периоду, а наведене вредности показују.
Литиј, формирањем металних веза, његов радијус је металик; и флуор, пошто формира ковалентне везе (Ф-Ф), његов радијус је ковалентан.
А ако желите да изразите атомски радио у јединицама ангстрома? Једноставно их поделите са 100: (257/100) = 2.57А. И тако даље са осталим вредностима.
Референце
- Цхемистри 301. Атомиц Радии. Добављено из: цх301.цм.утекас.еду
- Фондација ЦК-12. (28. јун 2016. године). Атомиц Радиус. Преузето са: цхем.либретектс.орг
- Трендови у атомским радијима. Преузето из: интро.цхем.окстате.еду
- Цлацкамас Цоммунити Цоллеге. (2002). Атомиц Сизе. Преузето са: дл.цлацкамас.еду
- Цларк Ј. (август 2012). Атомски и ионски полупречник. Преузето са: цхемгуиде.цо.ук
- Схивер & Аткинс. (2008). Неорганска хемија (Четврто издање, стр. 23, 24, 80, 169). Мц Грав Хилл.


