Калцијум фосфат (Ца3 (ПО4) 2) структура, својства, формација и употреба
Тхе калцијум фосфат је неорганска и терцијарна со чија је хемијска формула Ца3(ПО4)2. Формула наводи да је састав ове соли 3: 2 за калцијум и фосфат, респективно. Ово се може видети директно на доњој слици, где је приказана ознака2+ и анион ПО43-. За сва три Ца2+ Постоје два ПО43- с њима.
С друге стране, калцијум фосфат се односи на низ соли које варирају у зависности од Ца / П односа, као и степена хидратације и пХ. У ствари, постоје многе врсте калцијум фосфата које постоје и које се могу синтетизовати. Међутим, дословно поштујући номенклатуру, калцијум фосфат се односи само на трикалцијум, наведен.

Сви калцијум фосфати, укључујући Ца3(ПО4)2, Чврсто су бијеле боје са благим сивкастим тоновима. Они могу бити гранулирани, фини, кристални, и величине честица су око микрометара; и чак су припремљене наночестице ових фосфата, са којима су пројектовани биокомпатибилни материјали за кости.
Ова биокомпатибилност је последица чињенице да се те соли налазе у зубима и, укратко, у коштаном ткиву сисара. На пример, хидроксиапатит је кристални калцијум фосфат, који заузврат интерагује са аморфном фазом исте соли..
То значи да постоје аморфни и кристални калцијум фосфати. Из тог разлога, различитост и вишеструке опције нису изненађујуће када се синтетишу материјали на бази калцијум фосфата; Материјали у чијим својствима истраживачи су више заинтересовани сваког дана широм света да се фокусирају на обнову костију.
Индек
- 1 Структура калцијум фосфата
- 1.1 Аморфни калцијум фосфат
- 1.2 Остатак породице
- 2 Физичка и хемијска својства
- 2.1 Имена
- 2.2 Молекуларна тежина
- 2.3 Физички опис
- 2.4 Укус
- 2.5 Тачка топљења
- 2.6 Растворљивост
- 2.7 Густина
- 2.8 Индекс рефракције
- 2.9 Стандардна енталпија тренинга
- 2.10 Температура складиштења
- 2.11 пХ
- 3 Обука
- 3.1 Калцијум нитрат и амонијум хидроген фосфат
- 3.2 Калцијум хидроксид и фосфорна киселина
- 4 Усес
- 4.1 У коштаном ткиву
- 4.2 Биоцерамиц Цементс
- 4.3 Доктори
- 4.4 Остало
- 5 Референце
Структура калцијум фосфата
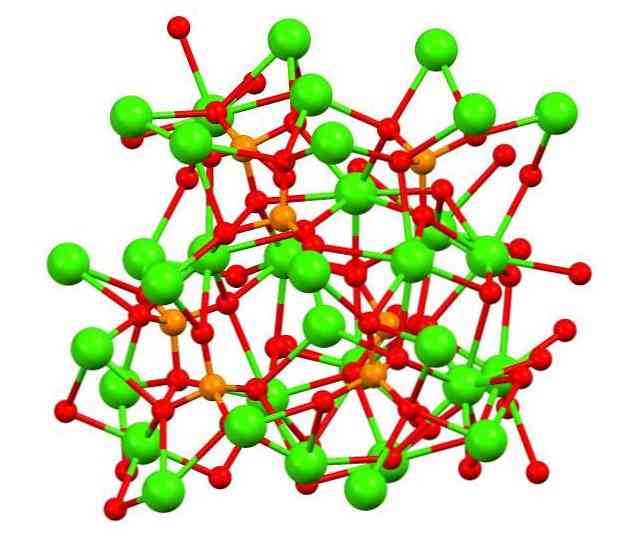
Горња слика приказује структуру трибазичног фосфата калика у чудном минералу вхитлоцките, који може садржати магнезијум и гвожђе као нечистоће..
Иако на први поглед може изгледати сложено, потребно је појаснити да модел претпоставља ковалентне интеракције између атома кисеоника фосфата и металних центара калцијума.
У репрезентацији је валидна, међутим, интеракције су електростатичке; то јест, катиони Ца2+ привлаче ПО аниони43- (Ца2+- О-ПО33-). Имајући ово на уму, разумљиво је зашто су на слици калциј (зелене сфере) окружени негативно набијеним атомима кисеоника (црвене сфере).
Када има толико иона, не оставља видљив симетрични распоред или образац. Тхе Ца3(ПО4)2 Усваја се на ниским температурама (Т<1000°C) una celda unitaria correspondiente a un sistema cristalino romboédrico; a este polimorfo se le conoce con el nombre de β-Ca3(ПО4)2 (β-ТЦП, за акроним на енглеском).
На високим температурама, с друге стране, трансформише се у полиморф α-Ца3(ПО4)2 (α-ТЦП), чија јединична ћелија одговара моноклинском кристалном систему. На још вишим температурама може се формирати и полиморф α'-Ца3(ПО4)2, који је од шестоугаоне кристалне структуре.
Аморфни калцијум фосфат
Кристалне структуре су поменуте за калцијум фосфат, што се може очекивати од соли. Међутим, она је способна да показује неуређене и асиметричне структуре, више повезане са типом "калцијум фосфатног стакла" него са кристалима у строгом смислу њене дефиниције..
Када се то деси, каже се да калцијум фосфат има аморфну структуру (АЦП, аморфни калцијум фосфат). Неколико аутора указује на ову врсту структуре као одговорну за биолошка својства Ца3(ПО4)2 у коштаном ткиву, могућа је његова поправка и биомиметизација.
Објашњавањем његове структуре нуклеарном магнетном резонанцом (НМР), пронађено је присуство ОХ јона- и ХПО42- у АЦП. Ови јони настају хидролизом једног од фосфата:
ПО43- + Х2О <=> ХПО42- + ОХ-
Као резултат тога, права структура АЦП-а постаје све сложенија, чији састав је представљен формулом: Ца9(ПО4)6-к(ХПО4)к(ОХ)к. 'Кс' означава степен хидратације, јер ако је к = 1, онда би формула била: Ца9(ПО4)5(ХПО4) (ОХ).
Различите структуре које ПЦА може зависити од моларних односа Ца / П; то јест, од релативних количина калцијума и фосфата, које мењају све њихове настале саставе.
Остатак породице
Калцијум фосфати су у ствари фамилија неорганских једињења, која заузврат могу да ступају у интеракцију са органском матрицом.
Други фосфати се добијају "једноставно" променом аниона који прате калцијум (ПО43-, ХПО42-, Х2ПО4-, ОХ-), као и врста нечистоћа у чврстом материјалу. Тако, до једанаест калцијум фосфата или више, сваки са својом структуром и својствима, може да настане природно или вештачки..
Испод су неки фосфати и њихове структуре и хемијске формуле:
-Водоник калцијум фосфат дихидрат, ЦаХПО4Х 2Х2О: моноклин.
-Калцијум дихидроген фосфат монохидрат, Ца (Х)2ПО4)2. Х2О: трицлиниц.
-Анхидровани диацид фосфат, Ца (Х)2ПО4)2: трицлиниц.
-Оцалциум хидроген фосфат (ОЦП), Ца8Х2(ПО4)6: трицлиниц Он је прекурсор у синтези хидроксиапатита.
-Хидрокиапатите, Ца5(ПО4)3ОХ: хексагонална.
Физичке и хемијске особине
Имена
-Калцијум фосфат
-Трицалциум фосфат
-Трицалциум дифосфат
Молекуларна тежина
310,74 г / мол.
Физички опис
То је бела чврста супстанца без мириса.
Тасте
Тастелесс.
Тачка топљења
1670 ºК (1391 ºЦ).
Растворљивост
-Практично нерастворљив у води.
-Нетопиво у етанолу.
-Растворљив у разблаженој хлороводоничној киселини и азотној киселини.
Густина
3,14 г / цм3.
Рефрацтиве индек
1,629
Стандардна енталпија тренинга
4126 кцал / мол.
Температура складиштења
2-8 ºЦ.
пХ
6-8 у воденој суспензији од 50 г / Л калцијум фосфата.
Траининг
Калцијум нитрат и водоник амонијум фосфат
Постоје бројне методе за производњу или формирање калцијум фосфата. Једна од њих се састоји од мешавине две соли, Ца (НО).3)2∙ 4Х2О, и (НХ4)2ХПО4, претходно растворени у апсолутном алкохолу и води. Једна со даје калцијум, а други фосфат.
Из ове смеше се АЦП таложи, који се затим подвргава загревању у пећи на 800 ° Ц и 2 сата. Као резултат ове процедуре добија се β-Ца3(ПО4)2. Пажљивим контролисањем температуре, агитације и времена контакта може доћи до формирања нанокристала.
Да се формира полиморф α-Ца3(ПО4)2 потребно је загрејати фосфат изнад 1000 ° Ц. Ово загревање се врши у присуству других металних јона, који стабилизују овај полиморф довољно да се користи на собној температури; то јест, остаје у стабилном мета стању.
Калцијум хидроксид и фосфорна киселина
Калцијум фосфат се такође може формирати мешањем раствора калцијум хидроксида и фосфорне киселине, са појавом киселинско-базне неутрализације. После пола дана зрења у матичним течностима, и њиховог правилног филтрирања, прања, сушења и просијавања, добија се гранулирани прах аморфног фосфата, АЦП.
Овај АЦП реагује на продукт високих температура, трансформишући се према следећим хемијским једначинама:
2Ца9(ХПО4) (ПО4)5(ОХ) => 2Ца9(П2О7)0.5(ПО4)5(ОХ) + Х2О (при Т = 446.60 ° Ц)
2Ца9(П2О7)0.5(ПО4)5(ОХ) => 3Ца3(ПО4)2 + 0.5Х2О (при Т = 748.56 ° Ц)
На овај начин добија се β-Ца3(ПО4)2, најчешћи и стабилнији полиморф.
Усес
У коштаном ткиву
Тхе Ца3(ПО4)2 То је главни неоргански састојак коштаног пепела. То је компонента трансплантата за замену костију, што се објашњава његовом хемијском сличношћу са минералима присутним у костима.
Биоматеријали калцијум фосфата се користе за исправљање дефеката кости и за облагање протеза од титанијума. На њима се таложи калцијум фосфат, изолујући их из околине и успоравајући процес титрације.
Калцијум фосфати, укључујући Ца3(ПО4)2, Користе се за производњу керамичких материјала. Ови материјали су биокомпатибилни и тренутно се користе за обнављање губитка алвеоларне кости, који је резултат пародонтних болести, ендодонтских инфекција и других стања..
Међутим, треба их користити само за убрзавање периапикалне поправке кости, у подручјима гдје нема хроничне бактеријске инфекције.
Калцијум фосфат се може користити у поправљању коштаних дефеката, када није могуће користити аутогени коштани графт. Могуће је користити га сам или у комбинацији са биоразградивим и ресорбујућим полимером, као што је полигликолна киселина..
Биоцерамиц цементс
Калцијум фосфатни цемент (ЦПЦ) је још један биокерамик који се користи у поправљању коштаног ткива. Производи се мешањем праха различитих врста калцијум фосфата са водом, формирајући пасту. Паста се може убризгати или прилагодити дефекту или шупљини кости.
Цементи су обликовани, постепено ресорбовани и замењени новонасталом кости.
Доцторс
-Тхе Ца3(ПО4)2 То је базична со, тако да се користи као антацид за неутрализацију вишка желучане киселине и повећање пХ вредности. У пасти за зубе обезбеђује извор калцијума и фосфата за олакшавање процеса реминерализације зуба и коштане хемостазе.
-Користи се и као додатак исхрани, иако је најјефтинији начин да се замени калцијум употребом карбоната и цитрата..
-Калцијум фосфат се може користити у лечењу тетаније, латентне хипокалцемије и терапије одржавања. Поред тога, корисна је у суплементацији калцијума током трудноће и дојења.
-Користи се у третману контаминације радиоактивним изотопима радио (Ра-226) и стронцијум (Ср-90). Калцијум фосфат блокира апсорпцију радиоактивних изотопа у дигестивном тракту, чиме се ограничава њихова штета.
Отхерс
-Калцијум фосфат се користи као храна за птице. Осим тога, користи се у зубним пастама за контролу зубног каменца.
-Користи се као средство против сљепљивања, на примјер, за спречавање збијања кухињске соли.
-Ради као средство за избељивање брашна. Док, у свињској масти свиња спречава нежељену боју и побољшава стање пржења.
Референце
- Тунг М.С. (1998) Калцијум фосфати: структура, састав, растворљивост и стабилност. У: Амјад З. (едс) Калцијум фосфати у биолошким и индустријским системима. Спрингер, Бостон, МА.
- Лангланг Лиу, Ианзенг Ву, Цхао Ксу, Суцхун Иу, Ксиаопеи Ву и Хонглиан Даи. (2018). "Синтеза, карактеризација нано-β-трикалцијум фосфата и инхибиција ћелија хепатоцелуларног карцинома", Јоурнал оф Наноматериалс, вол. 2018, Идентификациони број 7083416, 7 стр., 2018.
- Комби, Христ и Реј, хришћанин. (2010). Аморфни калцијум фосфати: синтеза, својства и употреба у биоматеријалима. Ацта Биоматериалиа, вол. 6 (бр. 9). пп. 3362-3378. ИССН 1742-7061
- Википедиа. (2019). Трицалциум фосфат. Преузето са: ен.википедиа.орг
- Абида и др. (2017). Трикалцијум фосфат у праху: Могућност припреме, карактеризације и збијања. Медитерранеан Јоурнал оф Цхемистри 2017, 6 (3), 71-76.
- ПубЦхем. (2019). Калцијум фосфат. Преузето са: пубцхем.нцби.нлм.них.гов
- Елсевиер (2019). Калцијум фосфат. Сциенце Дирецт. Преузето са: сциенцедирецт.цом


