Историја калориметра, делови, типови и њихове карактеристике
Тхе калориметар је уређај који се користи за мјерење промјене температуре неке твари (обично воде) познате специфичне топлине. Ова промена температуре је последица топлоте која се апсорбује или ослобађа у процесу који се проучава; хемикалија ако је реакција, или физичка ако се састоји од фазе или промјене стања.
У лабораторији, најједноставнији калориметар који се може наћи је онај шоље за кафу. Користи се за мерење топлоте која се апсорбује или ослобађа у реакцији при константном притиску, у воденом раствору. Реакције се бирају да би се избегла интервенција реагенса или гасовитих производа.
 У егзотермној реакцији, количина топлоте која се ослобађа може се израчунати из повећања температуре калориметра и воденог раствора:
У егзотермној реакцији, количина топлоте која се ослобађа може се израчунати из повећања температуре калориметра и воденог раствора:
Количина топлоте која се ослобађа у реакцији = количина топлоте коју апсорбује калориметар + количина топлоте коју апсорбује раствор
Количина топлоте коју апсорбује калориметар зове се калориметријски калорични капацитет. Ово се одређује снабдевањем познате количине топлоте калориметру са датом масом воде. Затим се мери повећање температуре калориметра и раствор који садржи.
Са овим подацима и коришћењем специфичне топлоте воде (4.18 Ј / г) може се израчунати калорични капацитет калориметра. Овај капацитет се назива и константом калориметра.
Са друге стране, топлота добијена воденим раствором је једнака м · це · Δт. У формули м = маса воде, це = специфична топлота воде и Δт = варијација температуре. Знајући све то, онда се може израчунати количина топлоте која се ослобађа егзотермном реакцијом.
Индек
- 1 Историја калориметра
- 2 Партс
- 3 Типови и њихове карактеристике
- 3.1 Шољица за кафу
- 3.2 Калориметријска пумпа
- 3.3 Адијабатски калориметар
- 3.4 Исопериболни калориметар
- 3.5 Калориметар протока
- 3.6 Калориметар за диференцијалну скенирајућу калориметрију
- 4 Апплицатионс
- 4.1 У физикохемији
- 4.2 У биолошким системима
- 4.3 Калориметар пумпе за кисеоник и калоријске снаге
- 5 Референце
Историја калориметра
Француски хемичар А. Л. Лавоисиер, 1780. године, који се сматра једним од очева хемије, користио је заморца да измери производњу топлоте својим дисањем.
Како? Коришћење уређаја сличног калориметру. Топлина произведена од заморца је доказана топљењем снијега који је окруживао апарат.
Истраживачи А.Л. Лавоисиер (1743-1794) и П.С. Лаплаце (1749-1827) дизајнирали су калориметар који је кориштен за мјерење специфичне топлине тијела методом топљења леда.
Калориметар се састојао од калајисане чаше с калајисом, лакиране, држане стативом и интерно завршене лијевком. Унутра је постављено још једно стакло, слично претходном, са цијеви која је пролазила кроз вањску комору и која је била опремљена кључем. Унутар другог стакла налазила се решетка.
У тој решетки је постављено биће или објекат чија је специфична топлота жељена. Лед је стављен у концентричне судове, као у кошари.
Топлота коју је тело произвело је апсорбована од стране леда, што је проузроковало његову фузију. Прикупљен је текући производ за топљење леда, отварајући кључ унутрашњег стакла.
И на крају, мерењем воде, позната је маса растопљеног леда.
Партс
Најчешће коришћени калориметар у наставним лабораторијама за хемију је тзв. Калориметар шоље. Овај калориметар се састоји од чаше, или уместо тога, контејнера аниме материјала који има одређена изолациона својства. Унутар овог контејнера водени раствор се ставља у тело које производи или апсорбује топлоту.
У горњем делу посуде постављен је поклопац изолационог материјала са два отвора. У једном се уводи термометар за мерење температурних промена, ау другом мешалица, пожељно од стакленог материјала, који обавља функцију померања садржаја воденог раствора..
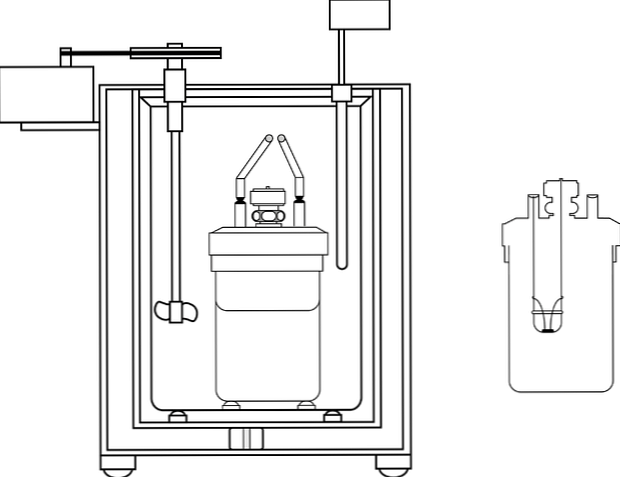
Слика приказује делове калориметријске пумпе; међутим, може се приметити да има термометар и мешалицу, заједничке елементе у неколико калориметара.
Типови и њихове карактеристике
Шољицу кафе
То је онај који се користи за одређивање топлоте која се ослобађа егзотермном реакцијом, а топлота која се апсорбује у ендотермној реакцији.
Поред тога, може се користити за одређивање специфичне топлоте тела; то јест, количина топлоте коју грам супстанце треба да апсорбује да би подигао своју температуру за један степен Целзијуса. .
Калориметријска пумпа
То је уређај у коме се мери количина топлоте која се ослобађа или апсорбује у реакцији која се одвија при константној запремини.
Реакција се одвија у јакој челичној посуди (пумпа), која је уроњена у велику количину воде. Због тога су промјене температуре воде мале. Према томе, претпоставља се да су промене повезане са реакцијом мерене на константној температури и запремини.
Горе наведено показује да се не обавља никакав рад када се реакција изводи у калориметријској пумпи.
Реакција започиње снабдевањем електричном енергијом преко каблова прикључених на пумпу.
Адијабатски калориметар
Одликује се изолацијом која се назива штит. Штит се налази око ћелије где се одвијају промене топлоте и температуре. Такође је повезан са електронским системом који одржава своју температуру веома близу температуре ћелије, како би избегао пренос топлоте.
У адијабатском калориметру, температурна разлика између калориметра и околине је минимизирана; као и минимизирање коефицијента преноса топлоте и времена за размену топлоте.
Његови делови се састоје од следећег:
-Ћелија (или контејнер), интегрисана у изолациони систем којим се покушава да избегне губитак топлоте.
-Термометар, за мерење температурних промена.
-Грејач, повезан са контролисаним извором електричног напона.
-И штит, већ споменут.
У овом типу калориметра могу се одредити особине као што је ентропија, дебејева температура и густоћа електронског стања.
Изориболички калориметар
То је уређај у којем су реакцијска ћелија и пумпа уроњени у структуру која се назива јакна. У овом случају, такозвана јакна се састоји од воде, која се држи на константној температури.
Температура ћелије и пумпа расту како се топлота ослобађа током процеса сагоревања; али температура водене јакне одржава се на фиксној температури.
Микропроцесор контролише температуру ћелије и јакне, правећи потребне корекције топлотне енергије која проистиче из разлике између две температуре.
Ове корекције се примењују непрекидно, и са коначном корекцијом, на основу мерења пре и после теста.
Калориметар протока
Развијен од стране Цалиендар, има уређај за помицање плина у контејнеру константном брзином. Приликом додавања топлоте мери се повећање температуре у течности.
Калориметар протока карактерише:
- Тачно мерење константне брзине протока.
- Прецизно мерење количине топлоте која се уноси у течност кроз грејач.
- Прецизно мерење пораста температуре гаса узрокованог уносом енергије
- Дизајн за мерење капацитета гаса под притиском.
Калориметар за диференцијалну скенирајућу калориметрију
Карактерише га поседовање два контејнера: у једном се поставља узорак који се испитује, док се други држи празним или се користи референтни материјал..
Два пловила се загријавају константном брзином енергије, помоћу два независна гријача. Када почне загревање два контејнера, компјутер ће графички приказати разлику топлотног протока грејача у односу на температуру и тако одредити проток топлоте.
Поред тога, може се одредити варијација температуре као функција времена; и на крају, капацитет калорија.
Апплицатионс
Ин пхисицоцхемистри
-Основни калориметри, тип шоље за кафу, дозвољавају да се измери количина топлоте коју тело ослобађа или апсорбује. Они могу одредити да ли је реакција егзотермна или ендотермна. Поред тога, може се одредити специфична топлота тела.
-Са адијабатским калориметром могуће је одредити ентропију хемијског процеса и електронску густину стања.
У биолошким системима
-Микрокалориметри се користе за проучавање биолошких система који укључују интеракције између молекула, као и молекуларне конформацијске промјене које се јављају; на пример, у развоју молекула. Линија укључује и диференцијално скенирање и изотермно титрирање.
-Микрокалориметар се користи у развоју лекова малих молекула, биотерапија и вакцина.
Калориметар пумпе за кисик и снагу калорија
Изгарање бројних супстанци се одвија у калориметру пумпе за кисеоник, а његова калоријска снага се може одредити. Међу испитиваним супстанцама кроз употребу овог калориметра су: угаљ и кокс; јестива уља, тешка и лагана; бензина и свих моторних горива.
Као и врсте горива за реакторе ваздухоплова; отпад од горива и одлагање отпада; прехрамбени производи и суплементи за људску исхрану; крмно биље и суплементи за сточну храну; грађевински материјали; ракетна и потисна горива.
Исто тако, калоријска снага је одређена калориметријом у термодинамичким студијама запаљивих материјала; у проучавању енергетског биланса у екологији; у експлозивима и термичким праховима и у настави основних термодинамичких метода.
Референце
- Вхиттен, Давис, Пецк & Станлеи. Цхемистри (8. изд.). ЦЕНГАГЕ Леарнинг.
- Гонзалез Ј., Цортес Л. & Санцхез А. (с.ф.). Адиабатска калориметрија и њене примене. Опорављено од: ценам.мк
- Википедиа. (2018). Цалориметер. Преузето са: ен.википедиа.орг
- Хелменстине, Анне Марие, Пх.Д. (22. јун 2018). Дефиниција калориметра у хемији. Преузето са: тхоугхтцо.цом
- Гиллеспие, Цлаире. (11. април 2018. године). Како калориметар функционише? Сциенцинг. Добављено из: сциенцинг.цом


